主な違い – 二酸化炭素と一酸化炭素
気体は、すべての物質が存在しうる3つの主要な状態のうちの1つです。
他の2種類は固体と液体です。
気体には、固体や液体にはないユニークな性質があります。
気体の分子は非常に小さく、気体分子間の相互作用はほとんどない。
室温ではさまざまな元素や分子が気体として存在する。
二酸化炭素と一酸化炭素はそのような気体です。
二酸化炭素と一酸化炭素の主な違いは、二酸化炭素が炭素原子1個に酸素原子2個で構成されているのに対し、一酸化炭素は炭素原子1個に酸素原子1個で構成されていることです。
二酸化炭素とは?
二酸化炭素は、分子式CO2で表される常温の気体です。
この気体は、生物の呼吸の際に放出されるため、非常にありふれたものです。
また、独立栄養生物の光合成過程の主要な構成要素でもあります。
二酸化炭素分子の分子質量は約44g/molです。
無色・無臭の気体です。
二酸化炭素の分子形状は直線的です。
炭素原子の両側に酸素原子が2つ、共有結合でくっついている。
1つのC=O結合の長さは約116.3pmです。
この分子は対称的です。
従って、これは双極子ではない。
(双極子とは、その分子内の結合の種類によって、原子に部分的に電荷を持つ分子のことである)。
炭素原子は黒色で、2つの酸素原子は赤色で示されている。
二酸化炭素は水によく溶け、炭酸(H2CO3)を生成する。
しかし、炭酸は水溶液中では弱酸であるため、一部がイオンに解離する。
したがって、水中では気体の二酸化炭素と炭酸は平衡状態にある。
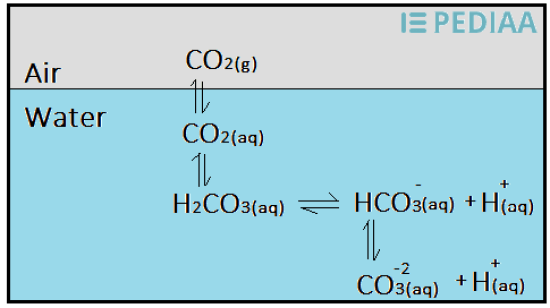 図02: 大気中の二酸化炭素は水に溶解することができる。
図02: 大気中の二酸化炭素は水に溶解することができる。
大気中の二酸化炭素の含有量は約0.03%であり、急速に増加していることが分かっています。
この増加は、主に化石燃料の燃焼と森林伐採が原因です。
化石燃料の燃焼による主な生成物の1つが二酸化炭素です。
大気中の二酸化炭素のほとんどは、森林に吸収されています。
つまり、二酸化炭素は樹木の光合成の過程で利用されるのです。
しかし、森林伐採によって、植物が取り込む二酸化炭素の量は減少します。
その結果、大気中の二酸化炭素の割合が上がってしまうのです。
しかし、二酸化炭素は温室効果ガスであるため、大気中の二酸化炭素の量が増えることは好ましくありません。
温室効果ガスは、赤外線を吸収したり放出したりすることができます。
そのため、地球温暖化が急速に進行してしまうのです。
一酸化炭素とは
一酸化炭素は、分子式COで表される常温の気体です。
炭素原子1個と酸素原子1個のみで構成されている。
したがって、その構造は基本的に直線的です。
酸素原子は炭素原子と共有結合している。
しかし、一酸化炭素は二酸化炭素と異なり、炭素と酸素の間に三重結合を持っています。
この三重結合は、二重結合と配位結合から構成されています。
二重結合が形成された後、酸素原子には2つの孤立電子対が存在します。
安定な分子を形成するためには、この孤立電子対のうちの1つを炭素原子に与える必要があります。
そうでない場合、炭素原子は八重項規則に従わず、2つの孤立電子対が互いに反発しあい、不安定な分子が形成される。
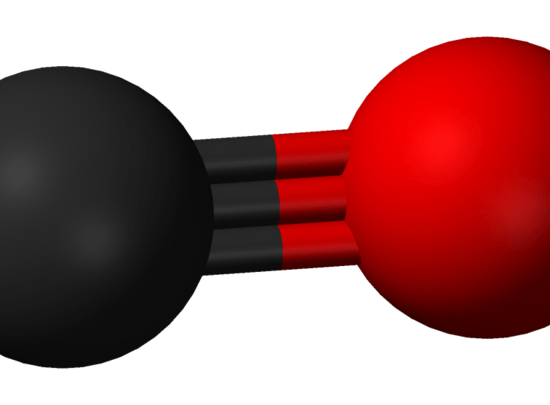 図03: 二酸化炭素の棒と玉の構造。
図03: 二酸化炭素の棒と玉の構造。
炭素原子は黒色、酸素原子は赤色で表示されている。
二酸化炭素は炭素と酸素の間に二重結合があるのに対し、一酸化炭素は炭素と酸素の間に三重結合があるため、炭素と酸素の結合長は約112.8pmと二酸化炭素より短くなる。
三重結合は二重結合よりも強固に結合しているため、結合長が短くなります。
酸素原子は炭素よりも電気陰性度が高いため、一酸化炭素分子にはわずかながら双極子モーメントが存在する。
しかし、炭素に電子を与える配位結合があるため、強い双極子ではありません(双極子の結果、炭素原子に部分的に正の電荷が生じ、酸素が与える電子でこの電荷をある程度中和することができます)。
一酸化炭素は大気中にごくわずかしか存在しない。
一酸化炭素は有毒ガスとして扱われる。
これは、血液中のヘモグロビン(酸素分子が結合する部分)と結合して、体細胞への酸素の運搬を阻害することがあるからです。
そのため、体内の細胞に十分な酸素が行き渡らなくなり、細胞を死に至らしめる可能性があります。
一酸化炭素は、化石燃料の不完全燃焼による副産物です。
乾燥した空気中に一酸化炭素が多く含まれる場合、それは汚染された空気とみなされる。
加熱した炭(カーボン)に二酸化炭素を通すと、一酸化炭素が発生する。
一酸化炭素は酸化して二酸化炭素になり、還元剤として働きます。
一酸化炭素の炭素の酸化状態は+2であり、二酸化炭素では+4に酸化されます。
それとは別に、一酸化炭素はCuO(酸化銅)から銅金属(Cu)を単離するのに使うことができます。
その反応を以下に示します。
CuO(s) + CO(g) → Cu(s) + CO2(g)となります。
一酸化炭素の主要な反応は、遷移金属との反応です。
この特徴を利用して、遷移金属元素の化合物から純粋な遷移金属元素を得ることができる。
二酸化炭素と一酸化炭素の違い
定義
二酸化炭素のこと。
二酸化炭素は、分子式CO2で表される常温の気体です。
一酸化炭素。
一酸化炭素は、分子式COで表される室温での気体です。
組成
二酸化炭素。
二酸化炭素は、炭素原子1個と酸素原子2個が結合したものです。
一酸化炭素。
一酸化炭素は、炭素原子と酸素原子1個が結合したものです。
モル質量
二酸化炭素の場合 二酸化炭素のモル質量は約44g/mol。
一酸化炭素。
一酸化炭素のモル質量は約28g/molです。
炭素-酸素結合長
二酸化炭素の場合 二酸化炭素では、炭素と酸素の結合長は約116.3pmです。
一酸化炭素。
炭素と酸素の結合長は約112.8pmの一酸化炭素。
ボンディング
二酸化炭 素。
二酸化炭素は、炭素と酸素の間に共有二重結合があります。
一酸化炭素。
一酸化炭素の炭素と酸素の間には、共有二重結合と配位結合(全部で三重結合)があります。
フォーメーション
二酸化炭素のこと。
化石燃料が完全に燃焼すると二酸化炭素が発生する。
一酸化炭素。
一酸化炭素は、化石燃料の不完全燃焼により発生します。
化学反応
二酸化炭素 二酸化炭素は酸化反応を起こすことができない。
一酸化炭素。
一酸化炭素は、酸化反応を起こすことができる。
結論
二酸化炭素は環境にとって有用なガスとされているが、増えすぎると地球温暖化の原因となるため好ましくない。
一酸化炭素は有毒ガスとされ、吸入すると血液中の酸素運搬が阻害され、細胞を死滅させる。
しかし、この2つのガスは大気中に微量に存在し、その割合は人間活動により急速に増加している。
二酸化炭素と一酸化炭素の主な違いは、その構造と組成にある。
