主な違い – スルホン化反応と硫酸化反応
スルホン化および硫酸化は、分子に含硫基を付加または置換する2つの化学反応です。
これらのプロセスは、さまざまな製品の製造に使用される主要な工業的化学プロセスです。
スルホン化とは、有機スルホン酸を調製する工程です。
このプロセスでは、三酸化硫黄、硫酸、クロロ硫酸などの化合物を有機化合物と反応させます。
また、スルホン化とは、C-O-S結合の形成を伴う重要な化学プロセスです。
スルホン化と硫酸化の主な違いは、スルホン化がC-S結合の形成を伴うのに対し、硫酸化ではC-O-S結合の形成を伴うことです。
スルホン化とは
スルホン化とは、有機化合物中の炭素にスルホン酸基(-SO3H)を直接結合させることである。
スルホン化反応の最終生成物はスルホン酸塩と呼ばれる。
スルホン化反応では、有機化合物が三酸化硫黄(SO3)、硫酸(H2SO4)、クロロ硫酸などの含硫酸性化合物と反応する。
スルホン化反応により、有機化合物の炭素原子の1つと含硫化合物の硫黄原子の間にC-S結合が形成される。
最終的に得られる化合物は酸性化合物であり、スルホン酸に分類される。
製造後、スルホン酸は安定であるため、単離・保存が可能である。
図1:ベンゼンのスルホン化反応
スルホン化反応は、非常に急速かつ極端な発熱反応であるため、工業的な利用は非常に困難です。
ほとんどの有機化合物は、この急激な反応と発熱により、三酸化硫黄と接触すると黒いチャーを形成する。
また、スルホン化によりスルホン酸に変換されると、有機化合物の粘度が非常に高くなる。
粘度が高くなると、反応混合物から熱を取り除くことが難しくなる。
そのため、適切な冷却操作が必要である。
そうしないと、副反応によって好ましくない副生成物が生成される可能性がある。
このような理由から、工業規模のスルホン化反応には特殊な装置が必要です。
一方、三酸化硫黄の反応性を制御することで、スルホン化反応の速さを緩やかにすることができる。
これには2つの方法があります。
- 希釈する
- 錯形成
三酸化硫黄の錯形成は、以下の方法で行うことができます。
- 三酸化硫黄とアンモニアを反応させてスルファミン酸を作る。
- 三酸化硫黄と塩酸を反応させてクロロ硫酸を作る。
- 三酸化硫黄と水を反応させてオレウムを作る。
したがって、これらの化合物のいずれか、あるいはいくつかを用いて硫酸化処理を行うことができる。
しかし、工業生産におけるスルホン化工程に使用する化合物の種類を選択する際には、いくつかの要因を考慮する必要があります。
以下にその例を挙げます。
- 要求される最終製品およびその品質
- 必要な生産能力
- 試薬のコスト
- 設備費
- 廃棄物処理費用
サルフェーションとは
硫酸化とは、有機化合物の水素原子を硫酸(-OSO2OH)官能基に置き換えることである。
この過程では、C-O-S結合が形成される。
しかし、最終生成物(硫酸塩と呼ばれる)は安定した生成物ではない。
簡単に分解して硫酸と別の化合物を形成してしまう。
したがって、硫酸化が進行した後は、系を中和する必要がある。
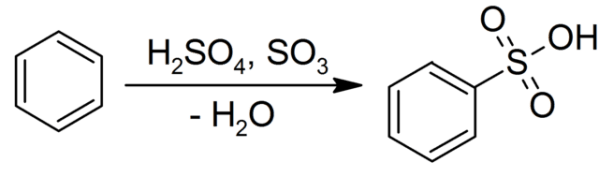 図2:赤丸内の化合物は、この系の硫酸化の生成物です。
図2:赤丸内の化合物は、この系の硫酸化の生成物です。
上の図は、硫酸化反応の様子です。
中和がうまくいっていないため、硫酸化反応の生成物が分解して硫酸になっています。
硫酸塩はその不安定性から、中性化合物としてしか存在しない。
生化学では、硫酸化とは酵素触媒によりスルホ基を他の分子に結合させることである。
この反応に関与する酵素は硫酸転移酵素と呼ばれる。
スルホン化と硫酸化の違い
定義
スルホン化。
スルホン化とは、有機化合物の炭素に直接スルホン酸基(-SO3H)を結合させることである。
スルフェーション。
有機化合物の水素原子を硫酸(-OSO2OH)官能基で置換することである。
ボンド形成
スルホン化。
スルホン化によりC-S結合が形成される。
硫酸化。
硫酸化によりC-O-S結合が形成される。
安定性
スルホン化。
スルホン化の最終生成物は安定です。
硫酸化反応。
硫酸化の最終生成物は不安定です。
ネーミング
スルホン化。
スルホン化の最終生成物は、スルホン酸塩またはスルホン酸と呼ばれる。
スルファチオン。
スルホン化の最終生成物は硫酸塩と呼ばれる。
稼働率
スルホン化。
スルホン化物は、反応混合物から単離された純粋な化合物として入手可能です。
スルフェート。
硫酸塩は、不安定であるため、中性化合物としてのみ入手可能である。
結論
スルホン化および硫酸化は、有機化合物に含硫基を付加するために多くの産業で使用される重要な化学プロセスです。
スルホン化と硫酸化の主な違いは、スルホン化ではC-S結合が形成されるのに対して、硫酸化ではC-O-S結合が形成されることです。
