主な違い – 価電子と自由電子の違い
原子は、電子、陽子、中性子の3種類の素粒子で構成されています。
陽子と中性子は原子の原子核の中にあります。
電子は原子核の外側にある。
この電子は原子核の周りを一定の距離で連続的に移動しています。
これらの電子が移動する経路を電子殻または軌道と呼びます。
1つの原子は1つまたは複数の軌道を持つことができます。
価電子とは、原子の一番外側の軌道に存在する電子のことです。
自由電子は、原子に束縛されていません。
これらの電子は、格子構造の中で見つけることができます。
格子内部で自由に動いています。
価電子と自由電子の主な違いは、電子の数が元素の特性であるのに対し、自由電子の数は格子の特性であることです。
価電子とは
原子の最外周の軌道に存在する電子のことです。
原子の原子核に対して最も引力が弱い電子です。
これは、価電子が原子の他の電子よりも長い距離に位置しているためです。
価電子は原子の化学反応や化学結合を担っている。
価電子と原子核の間の引力が小さいため、価電子は(内軌道の電子よりも)容易に除去することができる。
これは、イオン化合物や共有結合化合物を形成する際に重要です。
価電子を失うことで、原子は陽イオンを形成することができる。
原子の価電子を他の原子の価電子と共有することで、共有結合を形成する。
| — | — |
| 周期律表のグループ|価電子の数|||。
| 第1族(例:Na、K)|1|||。
| 2族(例:Ca, Mg)| 2||。
| 第13族(例:B、Al) 3個
| 第14族(例:C、Si)|4|5|6|7|8
| 15群(ex:N,P)・5群(ex:N,P)
| グループ16 (ex: O, S)
| 17族(ex:F, Cl)・・・7種
| グループ18(ex:He, Ne)| 8||。
sブロック元素とpブロック元素の場合、価電子は一番外側の軌道にある。
しかし、遷移元素の場合、価電子は内周の軌道にも存在することがあります。
これは、副軌道間のエネルギー差に起因する。
例えば、マンガン(Mn)の原子番号は25です。
コバルトの電子配置は[Ar]3d54s2です。
コバルトの価電子は4s軌道にあるはずです。
しかし、Mnには7個の価電子があります。
3d軌道は4s軌道の外側にあるため、3d軌道の電子も価電子とみなされます(3dのエネルギーは4s軌道より高い)。
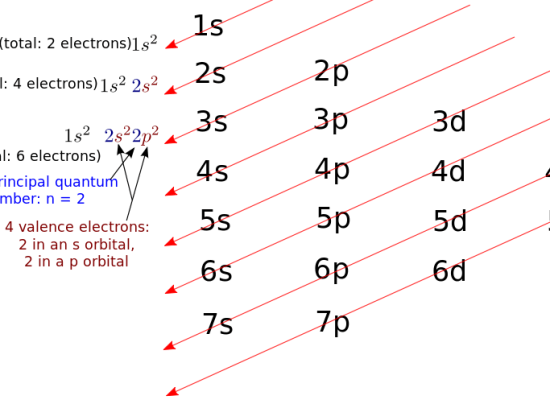 図1:炭素の価電子数
図1:炭素の価電子数
原子の酸化状態は、その原子の持つ価電子に依存する。
原子の中には、安定化するために価電子を取り除くものがあります。
その場合、その原子の酸化状態は増加する。
ある原子は、最外周の軌道にある電子をより多く獲得する。
すると、その原子の価電子の数が増えます。
その原子の酸化状態は減少する。
自由電子とは
自由電子とは、原子にくっついていない電子のことです。
自由電子はどこにでもあるわけではありません。
なぜなら、孤立電子は非常に反応性が高く、何にでも反応してしまうからです。
しかし、結晶構造や金属では、自由電子を見つけることができます。
自由電子とは、格子から離散化した電子のことです。
結晶構造では、結晶の欠陥によって、ある電子が定位置に留まらなくなることがあります。
この電子は自由電子となり、格子の中を自由に動き回ることができる。
この電子が、熱や電気の伝導を担っているのです。
金属では、金属イオンの間に自由電子が存在する。
自由電子の海の中に、金属イオンが格子状に並んでいるのです。
これらの自由電子は、金属を通して熱や電気を伝えることができる。
これらの自由電子は、金属を介して電流を流すことができます。
価電子と自由電子の違い
定義
価電子。
原子の最外周の軌道に存在する電子。
自由電子。
原子に付着していない電子のこと。
原子核への吸引力
価電子のこと。
価電子は原子核への吸引力が弱い。
自由電子。
自由電子は原子核に対して全く引力がない。
化学結合
価電子のこと。
価電子は原子の化学結合を担う。
自由電子。
自由電子は、化学結合には関与しない。
熱と電気の伝導
価電子のこと。
価電子は熱や電気を伝えることができない。
自由電子。
自由電子は、熱や電気を伝導させる。
自然
価電子の数。
価電子の数は元素の特性です。
自由電子。
自由電子の数は、格子の特性です。
結論
価電子とは、原子にゆるく結合している電子のことです。
自由電子は、どの原子にも全く束縛されていない電子です。
価電子は、原子の化学反応や化学結合に関与している。
自由電子は、格子構造の熱伝導や電気伝導に関与している。
価電子と自由電子の間には多くの違いがあります。
主な違いは、電子の数が元素の特性であるのに対し、自由電子の数は格子の特性であることです。
