主な違い – 求電子剤と求核剤
有機物や無機物の化学反応は、親電子物質と求核物質によって起こることがほとんどです。
親電子と親核は、原子や分子の誘導体として定義することができます。
親電子と親求核の主な違いは、親電子は電子対を受け取ることができる原子または分子であるのに対し、親核は電子対を供与することができる原子または分子であることです。
親電子物質とは
親電子体とは、電子を多く含む種から電子対を受け取り、共有結合を形成することができる原子または分子のことである。
親電子とは、電子を受け取るための自由な軌道を持つ、正または中性に帯電した原子や分子のことである。
親電子体は、電子を受け取る能力が高いため、ルイス酸と呼ばれる。
親電子体は、原子や分子が八分則に従うための電子を欠いていたり、安定になるために中和される必要のある正の電荷を持っている場合に作られます。
例えば、ヒドロニウムイオン(H3O+)は親電子体です。
正電荷を持ち、水素原子は電子を受け入れる自由空間を持っています。
したがって、-OHのようなルイス塩基から電子対を受け取り、H2O分子を形成することができる。
有機化学では、親電子体は付加反応や置換反応を起こす。
例えば、アルケンへのハロゲンの付加は親電子付加反応によって起こる。
図01:アルケンと臭素の付加反応
求電子置換反応には、分子の官能基を置き換える求電子剤の置換が含まれる。
ベンゼンを用いた親電子置換反応が最も一般的です。
図02: ベンゼンへの求電子剤の親電子置換反応。
親電子の強さは、親電子性によって決まる。
親電子性とは、親電子性物質の親電子性を示す用語で、親電子性物質がどのような性質を持つかを示す。
この親電子性は、親電子の電荷などに依存する。
求核剤とは
親核剤とは、電子対を提供できる原子や分子のことで、その能力からルイス塩基とも呼ばれる。
求核剤は親電子剤に電子を供与することができる。
π結合を持つ分子や自由電子対を持つ原子・分子は求核剤として働く。
求核剤は通常、負に帯電している。
電子豊富な原子を持つ中性荷電分子も求核物質として振る舞うことがあります。
また、求核剤は、求核付加反応や求核置換反応などの特異な反応を示す。
上の例は、求核剤と求電子剤の反応です。
ここでは、H2O分子が求核剤として作用する。
正電荷を持つカルボカチオンに電子を与える。
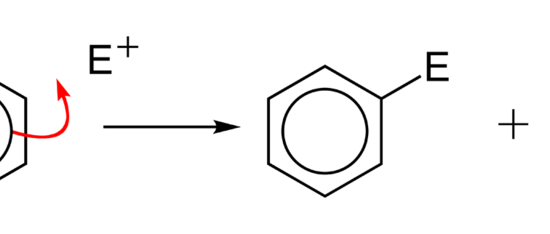 図04:求核置換反応
図04:求核置換反応
上の図は、求核置換反応です。
求核剤は「Nu」で示され、ベンゼン環の官能基「X」が求核剤で置換される。
そして、求核剤はベンゼン環に結合し、「X」基はベンゼン環から離脱する。
したがって、「X」は脱離基と呼ばれる。
親核性とは、求核剤に関する重要な用語です。
親核性とは、ある特定の求核剤の強さを決めるものです。
この求核性は、電荷、塩基性、分極性など多くの要因に依存する。
例えば、求核剤の負の電荷が増加すると、求核性が増加する。
つまり、負の電荷を多く持つ求核剤は、優れた求核剤として作用する。
親電子と求核の違い
定義
親電子体。
求電子性: 電子を多く含む種から電子対を受け取り、共有結合を形成することができる原子または分子のこと。
求核剤。
求核剤:電子対を供与することができる原子または分子。
電荷
親電子体。
親電子体は、正電荷または中性電荷を持つ。
求核剤。
求核剤は、負電荷または中性電荷を帯びる。
化学反応
親電子体。
求電子:親電子付加反応や親電子置換反応を起こす。
求核剤。
求核剤:求核付加反応や求核置換反応を起こす。
その他の名称
親電子体。
親電子体はルイス酸とも呼ばれる。
求核剤。
求核剤は、ルイス塩基とも呼ばれる。
結論
有機化学や無機化学の化学反応では、親電子と求核子が大きな役割を果たす。
親電子と求核の主な違いは、親電子は電子対を受け取ることができる原子または分子であるのに対し、求核は電子対を供与することができる原子または分子であることである。
