主な違い – pKa vs pH
物理化学では、pKaとpHは系の酸性度に関連する2つの用語です。
これらは対数値です。
非常に大きな量や非常に小さな量を表現したり比較したりする最も簡単な方法は、それらの対数値を取ることです。
対数で表すとシンプルな値になり、非常に扱いやすくなります。
pKaとpHの主な違いは、pKaが酸の解離を示すのに対し、pHは系の酸性度またはアルカリ性を示すことです。
pKaとは
pKa is the negative value of the logarithm of Ka. Ka is the symbol given for acid dissociation constant. Some acids are strong acids while some are weak acids. Strong acids completely dissociate into its ions when it is in aqueous solutions. But weak acids partially dissociate, generating an equilibrium between the acid and its conjugated base. For example, if we consider a weak acid named HA, its dissociation can be given as below. 
この平衡の酸解離定数は
Ka = [A-][H+]/[HA] です。
ここで
[A-] = 共役塩基の濃度
[H+]=H+イオンの濃度
[HA] = 存在する酸の濃度
とすると、酸解離定数のpKa値は、以下のように示すことができる。
pKa = – log10[Ka]となります。
pKaの値を見ることで、酸が強酸か弱酸かを判断することができます。
pKaの値が高ければ、その酸は弱酸です。
これは、pKaの値が高いほどKaが低いことを表しているからです。
Kaの値が低いためには、[A-][H+]の値が[HA]の値より低くなければなりません。
これは、酸が部分的に解離していることを意味します。
しかし、[A-][H+] の値が [HA] よりも高ければ、Ka は高くなり、それに対応して pKa も低くなります。
これは強酸であることを示しています。
pHとは
pH is the logarithmic value of the inverse of H+ concentration. pH value indicates the acidity or alkalinity of a system. If the pH value of a particular system is high, then it is called an alkaline or basic system. If the pH value of a system is low, that system is acidic. The range of pH is from 1 to 14. The pH value 7 is known to be the neutral pH where no acidity or alkalinity is present. The relationship between pH and pKa can be shown as below.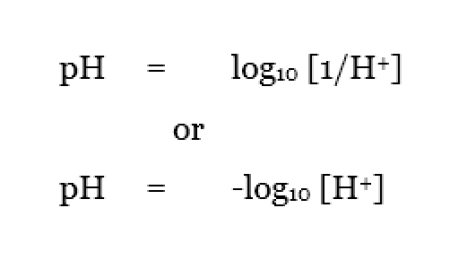
分析化学において、ある反応の終点を特定するためにpHインジケータが使用されます。
これらの指示薬はpHの変化に非常に敏感で、水溶液のpH値によって異なる色を示す。
pH計は、水や溶液のpHを測定するために使用されます。
pKaとpHの違い
定義
pKa: pKaはKaの対数の負の値です。
pH:pH は H+ 濃度の逆数の対数値。
酸性の表示
pKa:酸が強酸であるか弱酸であるかを示す。
pH:pH は酸性かアルカリ性かを示す。
詳細
pKa: pKaは、水溶液中の酸の解離の詳細を与える。
pH: pH は系内の H+ イオンの濃度についての詳細を与える。
値
pKaのこと。
酸のpKaが高ければ弱酸であり、低ければ強酸です。
pH:系のpHが高ければアルカリ性で、低ければ酸性です。
その他のパラメーターの影響
pKa: pKaは、酸、共役塩基、H+の濃度に依存する。
pH:pHはH+の濃度に依存する。
結論
pKaとpHは、どちらも実験実務において非常に重要なパラメータです。
pKaとpHの主な違いは、pKaが酸の解離を示すのに対し、pHは系の酸性度またはアルカリ性を示すことである。
