異性体は、その下に記載されている分子の幅広いコレクションを持っている有機化学の主要な分野の一つです。
異性化には、構造異性化と立体異性化の2種類があります。
キラリティーという概念は立体異性論に含まれる。
構造異性体とは異なり、立体異性体には、原子の構成は同じだが空間配置が異なる分子が含まれる。
キラリティーとは、ある分子の鏡像がその分子と重ね合わされないという性質です。
ある分子のキラリティーは、その分子に存在するキラル中心によって決定される。
有機化学では、不斉中心をキラルカーボンと呼ぶ。
キラルカーボンとは
キラルカーボンとは、非対称な炭素のことです。
炭素原子は最大4つの結合を持つことができます。
キラルカーボンは4つの異なる基と結合しています。
したがって、非対称です。
キラルカーボンであるためには、炭素原子が常にsp3混成している必要があります。
通常、不斉分子は少なくとも1つの不斉炭素を含んでいます。
spまたはsp2混成炭素原子は、π結合の存在により周囲に4つの異なる基を持つことができないので、不斉になることはできません。
不斉炭素原子を2個以上持つ分子は、1個の不斉炭素に対して2個の立体異性体を持つことになる。
したがって、その種の分子は2つ以上の立体異性体を持つことができる。
例えば、2つの不斉炭素を持つ分子は、各不斉炭素あたり2つずつ、計4つの立体異性体を持つことになる。
キラルカーボンの見分け方
脂肪族構造におけるキラル炭素の同定方法
分子内に存在する不斉炭素は、以下の2つのステップで同定することができる。
ステップ1
キラル炭素と想定される原子を中心に、分子の形状を決定する。
- 炭素原子の周りの形状が四面体であれば、キラル炭素である可能性があります。四面体でない場合は、アキラルとなります。
ステップ2
その炭素原子に付いている4つの基が、互いに異なるかどうかを判断します。
- 四面体配置の炭素原子が4つの異なる基と結合していれば、それはキラル炭素です。
図1: キラル分子とその鏡像
上の例では、分子が四面体配置で、中心の炭素原子が4つの異なる原子に結合している。
したがって、この炭素はキラルカーボンです。
環構造における不斉炭素の見分け方
置換基を持つ環構造の場合、炭素原子のキラリティーは以下のように決定することができます。
次の例で考えてみよう。
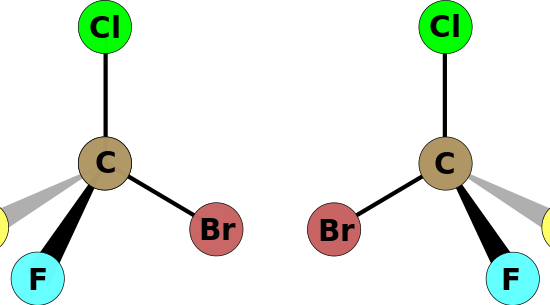 図2: メチルシクロヘキサン
図2: メチルシクロヘキサン
ステップ1
まず、その炭素原子に結合している基が互いに異なるかどうかを判断します。
もし異なっていれば、それは不斉炭素であると推測できる。
上の図では、この分子は同じ炭素原子に水素原子とメチル基が結合しています。
しかし、他の2つの基は環を形成しています。
ステップ2
環に含まれる2つの基を、環に含まれない仮想の基に変換する。
最も簡単な方法は、左側の不斉炭素と想定される原子と隣接する炭素原子との間の結合を切断し、それを配位子として想像することである。
次に、右側の隣接する結合を切断して、もう一方の配位子として想像します。
ステップ3
ここで、仮定した不斉炭素原子がキラルなのかアキラルなのかを判断することができます。
上の分子を考えた場合、環構造に他の置換がないため、想定される配位子はどちらも同じものです。
従って、仮定した炭素原子はアキラルです。
キラルカーボンの識別が重要な理由
不斉炭素の同定は、分子がキラルであるかアキラルであるかを説明します。
分子内に存在する不斉炭素の数を決定することは、その分子が持ちうる立体異性体の数を示す鍵となる。
これらの立体異性体は、分子と重ね合わせることができない。
従って、同じ構造を持つ異なる分子についての情報を与える。
概要
脂肪族構造や環構造の分子に含まれる不斉炭素原子の見分け方について説明します。
不斉炭素の存在は、立体異性体を持つことを示す。
これは、分子の関係や反応を観察する上で非常に重要です。
