主な違い – アポトーシスとネクローシス
アポトーシスとネクローシスは、多細胞生物において細胞死に関与する2つのメカニズムです。
アポトーシスは自然に起こる生理的なプロセスと考えられているのに対し、ネクローシスは毒物、外傷、感染症などの外的要因によって引き起こされる病理学的なプロセスであるとされています。
アポトーシスは高度に制御されたタイムリーなプロセスであるのに対し、ネクローシスは無秩序でランダムなプロセスです。
ネクローシスでは、炎症と組織損傷が観察されます。
アポトーシスとネクローシスの主な違いは、アポトーシスがあらかじめ定められた細胞の自殺であり、細胞が積極的に自滅して体内の機能を円滑に保つのに対し、ネクローシスは細胞の外部環境における制御不能な外部要因によって起こる偶発的な細胞死である点です。
本稿では、その実態を探る。
- アポトーシスとは
– 定義、特徴、プロセス - 壊死(ネクローシス)とは
– 定義、特徴、プロセス - アポトーシスとネクロシスの違いは?
アポトーシスとは
アポトーシスとはプログラムされた細胞死(PCD)のことで、生物の成長・発達に伴う規則的かつ制御されたメカニズムです。
細胞自殺とも呼ばれ、この過程では、細胞自身が死に関与している。
アポトーシスは、細胞の増殖のバランスを保つことを可能にする。
つまり、体内のひとつひとつの細胞は、自己の生命を持っているのだ。
例えば、赤血球は120日しか生きられないが、アポトーシスによって体内で自滅する。
アポトーシスは、明確に定義された、結果としての形態変化を通じて起こる。
細胞は乾燥によって収縮し、凝縮し、最後に断片化される。
核内のクロマチンの凝縮は、アポトーシスの特徴です。
アポトーシス小体と呼ばれる小さな膜結合小胞が形成され、細胞の内容物を含む。
したがって、アポトーシス時には、細胞内容物の細胞外への放出は観察されず、炎症反応も発生しない。
一方、ネクローシスにおける組織損傷に対応した細胞死は、アポトーシスとは異なる形態的変化を示す。
ネクローシスとは
ネクローシスとは、細胞死の一種で、正常な状態とは異なる極限状態に細胞が強くさらされることによって起こるものです。
極端な条件下では、細胞内環境にダメージを与え、細胞や組織に急激なダメージを与える。
したがって、ネクローシスは、受動的で偶発的な細胞死として特徴づけられる。
ネクローシスの間、細胞内容物は細胞外環境に放出され、隣接する細胞に有害な影響を発生させる。
形態学的に異なる6種類のネクローシスが確認できる。
- 凝固性ネクローシス
- 液状化壊死
- 壊疽性壊死
- カゼイン性壊死
- 脂肪壊死
- フィブリノイド壊死
機械的外傷、血管の損傷、虚血、極端な高温や低温のような熱作用によって引き起こされます。
また、クモに刺された場合も壊死の原因となることがあります。
図2に乳房リンパの脂肪壊死を示す部位を示します。
壊死した脂肪細胞の周囲に炎症反応が起こり、コレステロールの裂け目ができているのがわかる。
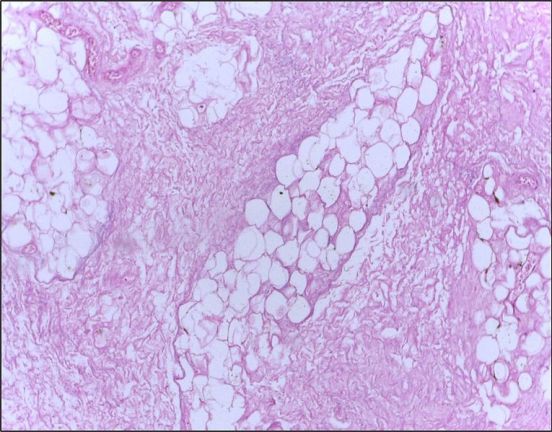 :図2 脂肪壊死
:図2 脂肪壊死
アポトーシスとネクローシスの違い
定義
アポトーシス。
アポトーシスは「プログラムされた」細胞死です。
ネクローシス(壊死)。
ネクローシスとは、「早すぎる」細胞死です。
プロセス
アポトーシス。
細胞質が収縮し、核が凝縮することでアポトーシスが起こる。
ネクローシス。
細胞質がミトコンドリアとともに膨張し、細胞が溶解する。
原因
アポトーシス。
アポトーシスは、自然に起こる生理的なプロセスです。
ネクローシス 壊死は、毒物、外傷、感染症などの外的要因によって引き起こされる病理学的プロセスです。
メンブレン インテグリティ
アポトーシス。
アポトーシス時には、細胞膜の完全性は失われないが、ブリービングが観察される。
ネクローシス。
ネクローシス:細胞膜の完全性が損なわれる。
クロマチン
アポトーシス。
アポトーシス:クロマチンはアポトーシスの際に凝集する。
ネクローシス。
ネクローシス:ネクローシス時にクロマチンに構造変化は見られない。
小器官
アポトーシス。
アポトーシスの際、ミトコンドリアは膜に孔をあけ、漏出する。
細胞死後も細胞内の小器官は機能している。
ネクローシス。
ネクローシスでは、細胞内小器官が膨張して分解される。
壊死した細胞内の小器官は、細胞死後も機能しない。
ミトコンドリアとライソゾーム
アポトーシス。
アポトーシス:ミトコンドリアは漏出するが、リソソームの機能は維持される。
ネクローシス。
ネクローシス:ミトコンドリアはそのままで、ライソゾームが漏出する。
ベシクル形成
アポトーシス アポトーシスにより、膜結合型の小胞(アポトーシス小体)が形成され、細胞は小体に断片化される。
ネクローシス。
小胞は形成されないが、完全な細胞溶解が起こり、細胞内容物が細胞外液に放出され、ネクロシスとなる。
レギュレーション
アポトーシス。
アポトーシスは、酵素による経路の活性化によって厳密に制御されている。
ネクローシス。
ネクローシスは制御不能なプロセスです。
カスパーゼ
アポトーシス。
アポトーシスはカスパーゼに依存する経路です。
ネクローシス。
壊死はカスパーゼ非依存的な経路です。
エネルギー必要量
アポトーシス。
アポトーシスは能動的なプロセスであり、ATPエネルギーを必要とする。
ネクローシス。
ネクローシスは不活性なプロセスであるため、このプロセスにはエネルギーは必要ない。
4 ℃での発生率
アポトーシス。
アポトーシスは活性プロセスであるため、4℃では発生しない。
ネクローシス。
ネクローシスは4℃で起こる。
DNAの消化
アポトーシス。
アポトーシスでは、DNAの非ランダムな一本鎖およびオリゴヌクレオソーム長の断片化が起こります。
これらのDNA断片はアガロースゲル電気泳動でバンドパターンを示す。
ネクローシス。
細胞内のDNAは、ネクローシスの際にランダムに消化される。
アガロースゲル電気泳動では、ランダムに消化されたDNAはスメアとなる。
DNA消化のタイミング
アポトーシス アポトーシスでは、前段階のDNA断片化が起こる。
ネクローシス。
ネクローシス:ネクローシスでは分解後のDNAが消化される。
細胞質への因子の放出
アポトーシス アポトーシス時には、ミトコンドリアからシトクロムCやAIFなどの様々な因子が死にかけた細胞の細胞質内に放出される。
ネクローシス。
細胞質内への因子の放出はない。
発生状況
アポトーシス アポトーシスは局所的なプロセスであり、個々の細胞を破壊することになる。
壊死(ネクローシス)。
壊死は連続した細胞群に影響を与える。
ファゴサイトーシス
アポトーシス。
アポトーシス:アポトーシス細胞は、食細胞や隣接する細胞によって貪食される。
壊死(ネクローシス) 壊死した細胞は貪食細胞によってのみ貪食される。
症状
アポトーシス。
炎症も組織障害も起こらない。
ネクローシス。
壊死:生体の免疫系により、著しい炎症反応が生じる。
ネクローシスは組織障害を引き起こす可能性がある。
影響力
アポトーシス。
アポトーシスは多くの場合、有益です。
しかし、異常な活性は病気を引き起こす可能性がある。
ネクローシス。
壊死は常に生体に有害です。
治療しない場合、致命的となることもあります。
機能
アポトーシス。
アポトーシス:多細胞生物の体内における細胞数の制御に関与する。
ネクローシス(壊死)。
組織の損傷や免疫系の誘導に関与し、病原体から体を守る。
結論
アポトーシスとネクローシスは、多細胞生物に見られる2つの細胞死のバリエーションです。
アポトーシスとネクローシスの主な違いは、細胞死に関与するメカニズムです。
アポトーシスは自然な生理的プロセスであるのに対し、ネクローシスは毒物、外傷、感染症などの外的要因によって引き起こされる病理学的プロセスです。
アポトーシスは体内の細胞数の制御に関与し、ネクローシスは免疫システムの誘導に関与して、病原体から体を守る。
アポトーシスを起こさない細胞は、腫瘍や癌の形成につながる。
アポトーシスの割合が増えると、心臓、肝臓、エイズなどの疾病につながる。
壊死は、細胞が毒素、温度上昇、酸素濃度の低下などの極限状態にさらされることによって損傷を受けたときに起こります。
また、組織の損傷や炎症にもつながる。
真核細胞の死滅の機構的説明”. Infection and Immunity. アメリカ微生物学会, 2005年4月. Web. 02 Apr. 2017.
2. Lodish, Harvey. “細胞死とその制御”. 分子細胞生物学. 第4版. 米国国立医学図書館、1970年1月1日。
Web. 02 Apr. 2017.
3. Alberts, Bruce. “プログラムされた細胞死(アポトーシス)”. 細胞の分子生物学. 第4版. 米国国立医学図書館、1970年1月1日。
