主な相違点 – 可逆過程と不可逆過程
熱力学では、ある系の挙動を表すのに可逆的と不可逆的という言葉が使われます。
ここで、その系で起こる過程を可逆過程と不可逆過程のどちらかと名付けることができる。
可逆過程と不可逆過程の主な違いは、可逆過程が逆にして初期状態を得ることができる熱力学的過程であるのに対し、不可逆過程は逆にしてシステムの初期状態を得ることができない熱力学的過程であることである。
可逆プロセスとは
可逆過程とは、ある系の初期状態を得るために逆戻りすることができる過程のことである。
ある化学反応(過程)が終了すると、系の初期状態が変化する。
つまり、系がある過程を経ることで、系は初期状態から最終状態に変化する。
もし、その過程を逆にして初期状態に戻せるなら、その過程を可逆過程と呼ぶ。
例えば、システムの初期状態をA、最終状態をBとしたとき、この変化を引き起こしたプロセスを逆行させることができれば、このプロセスは可逆プロセスであると言える。
ただし、この逆過程では元の状態Aが得られるはずで、周囲の性質は変わらない(熱力学的な性質が変わらない)はずです。
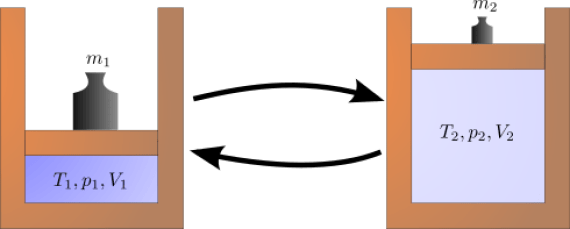 図01: 可逆過程
図01: 可逆過程
可逆過程は、完全に元に戻すことができ、その過程を経た痕跡を残さない初期状態に戻すことができる。
可逆過程が発生するためには、2つの重要なことがあります。
1.無限大に小さい時間で起こること。
つまり、測定もできないような時間でプロセスが起こること。
システムの初期状態と最終状態が互いに平衡であること。
そうでなければ、プロセスは可逆ではない。
不可逆プロセスとは
不可逆過程とは、熱力学的な過程のうち、ある系の初期状態を得るために逆戻りすることができない過程のことである。
つまり、ある系が不可逆過程を経ると、その系は最終状態に変化してしまい、過程を逆行させても初期状態を得ることはできない。
自然界で起こる過程のほとんどが不可逆的であることから、このような過程は自然過程とも呼ばれる。
不可逆過程は起こるまでに測定可能な時間がかかり、その系には平衡が存在しない。
不可逆的なプロセスによって系のエントロピーが変化し、この変化は元に戻すことができない。
不可逆的過程は、平衡から離れる熱力学的過程と表現できる。
ここでは、有限の変化が起こる。
不可逆過程の例としては、高いところから低いところへの水の流れ、暖かいところから冷たいところへの熱の流れ、真空系への気体の放出、などがあります。
可逆プロセスと非可逆プロセスの違い
定義
可逆過程。
可逆過程とは、あるシステムの初期状態を得るために逆戻りすることができる過程です。
不可逆過程。
不可逆過程とは、系の初期状態を得るために逆戻りすることができない熱力学的過程のこと。
リバーシブル
可逆的なプロセス。
可逆的なプロセスは、元に戻すことができる。
非可逆プロセス。
不可逆的なプロセスは、元に戻すことができない。
システムの変更点
可逆プロセス。
可逆プロセス:可逆プロセスでシステム内に無限の変化が起こる。
非可逆過程。
不可逆過程では、有限の変化が起こる。
均衡
可逆過程。
可逆過程が起こった系では、初期状態と最終状態の間に平衡が存在する。
不可逆的過程。
不可逆過程が起こった系では、平衡は存在しない。
結論
可逆過程と不可逆過程は、熱力学系で起こりうる熱力学的な過程です。
可逆過程と不可逆過程の主な違いは、可逆過程が逆にして初期状態を得ることができる熱力学的過程であるのに対し、不可逆過程は逆にして系の初期状態を得ることができない熱力学的過程であるということである。
