主な相違点 – アリール vs フェニル
フェニル基とアリール基は、有機化合物の官能基の名称として使用される2つの化学用語です。
アリール基は常に芳香環を含んでいます。
アリール基は、水素原子を1つ取り除いた単純な芳香族化合物であり、炭素鎖に結合することが可能です。
フェニルは側鎖に付けられた名前です。
ベンゼン環から水素原子を1つ取り除いたものです。
フェニル基は分子の側鎖として空いているところに付くことができます。
アリール基とフェニル基の主な違いは、アリール基という用語があらゆる芳香族官能基の名称に用いられるのに対し、フェニルという用語はベンゼン環に由来する官能基の名称に用いられる点です。
アリールとは
アリール基は、常に芳香環を含んでいます。
アリール基は単純な芳香族化合物で、環から水素原子を1つ取り除き、炭素鎖に結合できるようにしたものです。
最も一般的な芳香環はベンゼンです。
すべてのアリール基はベンゼン構造から派生している。
アリール基の例としては、ベンゼンから誘導されるフェニル基、ナフタレンから誘導されるナフチル基があります。
これらのアリール基は、その芳香族構造中に置換基を有することができる。
例えば、トリル基はトルエンに由来し、トルエンはベンゼン環にメチル基が置換されたものです。
アリール基はすべて不飽和です。
つまり、アリール基の構造は二重結合で構成されている。
しかし、アリール基が持つ芳香環の種類はベンゼンだけではありません。
例えば、インドリル基は一般的なアミノ酸であるトリプトファンに結合したアリール基です。
下図は、ベンゼン環に由来するフェニル基です。
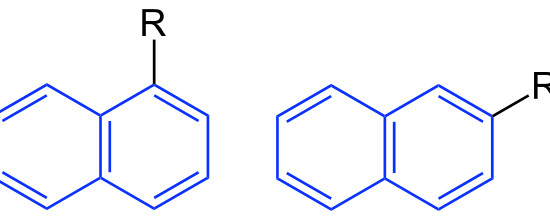 図1:青字の基はナフチル基
図1:青字の基はナフチル基
ハロゲン化アリールとは、芳香環のsp2混成炭素に直接ハロゲン原子が結合した分子です。
芳香環に二重結合があるため、不飽和な構造です。
ハロゲン化アリールも双極子-双極子相互作用を示す。
環電子が存在するため、炭素-ハロゲン結合はハロゲン化アルキルに比べて強い。
これは、芳香環が炭素原子に電子を与えるため、その正電荷がいくらか減少するためです。
ハロゲン化アリールは求電子置換が可能で、芳香環のオルト、パラ、メタの位置にアルキル基が付くことがある。
1個または2個のハロゲンが芳香環にくっつくことができる。
これもオルト位、パラ位、メタ位です。
フェニルとは
フェニルとは、ベンゼン環に水素原子を欠いた化学構造です。
水素原子がないため、他の原子や分子がフェニル基に結合するための空隙があります。
フェニルの化学式はC6H5です。
フェニル基は平面的な形状を持つ環状構造です。
ここでは、5つの炭素原子が5つの水素原子と個別に結合している。
残りの炭素原子には、水素原子は結合していない。
フェニル基は、対応する脂肪族アルキル基と比較すると、より安定です。
これは、π電子の非局在化により芳香環が安定化するためです。
フェニル基は、電子を共有する水素原子がないため、炭素原子の電子配置が不完全であり、単独では安定ではない。
このため、フェニル基は非常に反応性が高い。
フェニル基は電子が豊富な原子や原子団と反応することになる。
アリールとフェニールの違い
定義
アリール:アリール基は常に芳香環を含む。
フェニル ベンゼンから水素原子を1つ取り除いた化学構造。
フォーメーション
アリール:芳香族基から水素原子が抜けてアリール基となる。
フェニル ベンゼン環から水素が抜けてフェニル基となる。
炭素原子
アリール:アリール基の種類によって、炭素原子数が異なる場合があります。
フェニル フェニル基は6個の炭素原子からなる。
例
アリール基:アリール基の例としては、フェニル基、ナフチル基、トルイル基、インドリル基等が挙げられる。
フェニル基 フェニル基は、ベンゼン環から誘導される個々の基です。
結論
フェニル基は、アリール基の一種である。
アリール基は、有機化合物のうち芳香族に存在する官能基です。
アリール基とフェニル基の主な違いは、アリール基という用語があらゆる芳香族官能基の名称に用いられるのに対し、フェニルという用語はベンゼン環に由来する官能基の名称に用いられるという点です。
