主な違い – 水素 vs 酸素
元素周期表は、これまでに地球上で発見されたすべての元素を、原子番号の昇順に並べて表示したものです。
これらの元素の中には、地球上に非常に多く存在するものもあれば、微量にしか存在しないものもあります。
水素と酸素は、地球上のほとんどの場所に存在する元素です。
水素と酸素の主な違いは、水素は最も安定な同位体に中性子がないのに対し、酸素は最も安定な同位体に中性子が8個あることです。
水素とは?
水素は原子番号1、記号Hの元素で、周期表の一番上にある元素です。
水素には3つの自然発生同位体があります。
プロチウム、重水素、トリチウムです。
これらは原子核に含まれる中性子の数が互いに異なります。
これらの同位体のうち、最も多く存在するのがプロチウムです。
自然界に存在するプロチウムの濃度は約98%です。
したがって、一般的に水素といえばプロチウムのことを指します。
水素は中性子を持たず、陽子と電子を1つずつ持っています。
水素はs軌道を1つだけ持ち、他の軌道は持っていません。
したがって、水素原子が持つ唯一の電子はs軌道に位置しています。
この電子は単独で不対であるため、水素はこの電子を取り除くことで容易にH+イオンを形成することができます。
不対電子があると、水素原子は不安定になります。
そのため、水素はさまざまな元素と電子を共有して共有結合を形成する傾向があります。
自然界で最もよく見られる水素の形は、水の分子です。
水の分子では、2個の水素原子が1個の酸素原子と共有結合しています。
水の分子式はH2Oとなります。
それ以外にも、炭化水素、多くの一般的なポリマー、その他の有機物や無機物の中にも水素は含まれています。
水素は、大気中では水素ガスとして存在します。
水素ガスの分子式はH2です。
このとき、2つの水素原子は、それぞれが持つ唯一の電子を共有することによって、共有結合で結ばれています。
図01:HとH2の化学構造
標準的な温度と圧力では、水素は無色、無臭、無毒の気体です。
可燃性が高い。
H2ガスが金属元素と反応すると、H-アニオンを形成します。
この陰イオンをヒドリドと呼ぶ。
金属と水素化物との結合はイオン結合であり、水素原子は水素化物陰イオン中に2個の電子(ペア)を持っています。
酸素とは
酸素は、原子番号8、記号Oの元素です。
16O、17O、18O です。
しかし、最も多く存在するのは16Oです。
したがって、一般に酸素といえば、16Oの同位体を指すことになります。
酸素は原子核に8個の陽子と8個の中性子を持っています。
また、原子核の周囲に8個の電子を持っています。
これらの電子はs軌道とp軌道にあります。
酸素の電子配置は、1s22s22p4です。
電子を含む軌道の一番外側がp軌道であるため、酸素は周期表のpブロックに属します。
酸素は2p軌道に4個の電子を持っています。
そのうち2個の電子は対になっており、残りの2個の電子は対になっていません。
したがって、酸素は外から2個の電子を得ることでO2-アニオンを作ることができます。
2個の電子を得ると、酸素はネオンの電子配置になり、これは非常に安定な配置です。
酸素はO2ガスを形成します。
これは、すべての生物が呼吸するために必要な気体です。
大気中に含まれるO2ガスの割合は約21%です。
したがって、酸素は大気中に最も多く存在することになります。
また、酸素は水の分子にも含まれています。
そこでは、酸素原子が2つの水素原子と共有結合で結びついています。
酸素は、フッ素に次いで電気陰性度が高い元素です。
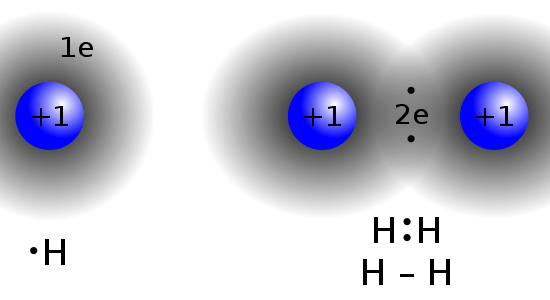 図02: O2分子の形成
図02: O2分子の形成
標準的な温度と圧力では、酸素は無臭、無色、無毒の2原子分子として存在する。
酸素にはO2とO3という2つの同素体があります。
O2は通常、二酸素または酸素と呼ばれるのに対し、O3はオゾンと呼ばれます。
オゾンは主に大気圏上層のオゾン層に存在する。
水素と酸素の違い
定義
水素:水素は原子番号1、記号Hの元素です。
酸素 酸素は、原子番号8、記号Oの元素です。
中性子の数
水素 最も一般的な水素の同位体には、原子核に中性子がない。
酸素 最も多い酸素の同位体は、原子核に8個の中性子を持つ。
軌道
水素:s軌道を1つだけ持つ。
酸素 酸素はs軌道とp軌道を持つ。
不対電子の数
水素:水素は不対電子を1個持つ。
酸素 酸素の不対電子は2個。
共有結合の数
水素: 水素は1つだけ共有結合を形成することができる。
酸素 酸素は2つの共有結合を形成することができます。
原子質量
水素 水素の原子質量は約 1.00794 u。
酸素 酸素の原子質量は15.999uです。
結論
水素も酸素も、地殻の中にたくさんあります。
そのため、水素と酸素の違いを理解することが重要です。
水素と酸素は、2原子分子として気体で存在するか、他の元素と結合して固体または液体で存在します。
