主な相違点 – 結合エネルギー vs 結合解離エネルギー
結合エネルギーと結合解離エネルギーは、どちらも 2 つの原子間の化学結合の破壊に関連するため、しばしば混同されるように思われる用語です。
結合エネルギーと結合解離エネルギーの概念は、通常、共有結合に関連して使用されます。
これは、共有結合がイオン結合と異なり、電子の共有によって形成される原子間の直接的な結合であるためです。
結合エネルギーと結合解離エネルギーの大きな違いは、結合エネルギーが化合物中の同じ2種類の原子間の結合をすべて分解するのに必要な平均的なエネルギー量を指すのに対し、結合解離エネルギーはホモリシスで特定の結合を分解するのに必要なエネルギー量であることである。
つまり、結合エネルギーは、同じ種類の原子間に存在するすべての結合の結合解離エネルギーの平均値です。
ボンドエネルギーとは
結合エネルギーとは、化合物中の同じ種類の原子間に存在するすべての結合を分解するのに必要なエネルギーの平均値として定義される。
通常、原子は互いに結合してエネルギーを下げ、より低いエネルギーレベルを得ようとする。
そうすることで、原子は安定になる。
結合するとき、ある一定のエネルギーが放出される。
このエネルギーは、多くの場合、熱として放出される。
したがって、結合を切断するためには、ある程度のエネルギーを与える必要がある。
結合エネルギーを計算する単位は kjmol-1 です。
同じ原子間に1本、2本、3本の結合がある分子では、結合エネルギーは異なる。
例えば、C-C単結合では、その結合を切るために347 kJmol-1の結合エネルギーが必要であるのに対し、C=C二重結合では614 kJmol-1の結合エネルギーが必要である。
しかし、C=Cに必要なエネルギー量は、C-C単結合のそれの2倍の値ではありません。
したがって、結合エネルギーは結合の種類によって異なるのです。
結合エネルギーと結合解離エネルギーの違いを考える上で、最も参考になるのが水(H2O)分子です。
H2O分子は、2つのO-H結合がH-O-Hとして結合した構造をしている。
H2Oの結合エネルギーは、H2O分子の2つのO-H結合を切断するのに必要なエネルギーの平均値である。
2つの結合は同じものですが、最初のO-H結合はH-OH構造から壊れるのに対し、2番目の結合は.O-Hとして壊れるので、エネルギー値はわずかに異なります。
酸素原子は水素原子よりも電気陰性なので、水分子からのO-H結合の切断は、酸素原子の両側の水素原子の有無に影響される。
したがって、その平均値を結合エネルギーとする。
結合解離エネルギーとは
結合解離エネルギーとは、ホモリシスにおいて特定の結合を分解するのに必要なエネルギー量と定義することができる。
化学結合の強さを表す。
結合解離エネルギーは、共有結合とも関係があります。
共有結合は、原子間で電子を共有することで形成されるため、結合の解離過程で共有された電子が原子に引き戻される。
したがって、生成するラジカルは不対電子を持つため、非常に反応性が高い。
こうして、ホモリシス開裂が起こる。
ここで同じH2Oを例にとると、H2O分子の結合解離により、下図のようにホモリシス開裂して.OHラジカルと.Hラジカルが生成されます。
H2O+エネルギー→.OH+.H
したがって、結合解離エネルギーで与えられているのは、-O-Hの1つの結合を切断するのに必要なエネルギーであり、したがって、-O-H結合の両方に対して同じ値が与えられているのである。
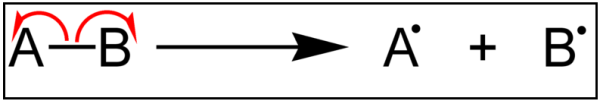 図2:化学結合のホモリシス
図2:化学結合のホモリシス
結合エネルギーと結合解離エネルギーの違い
定義
結合エネルギー。
結合エネルギーとは、化合物中の同じ2種類の原子間に存在するすべての結合を分解するのに必要な平均エネルギー量のことである。
結合解離エネルギー。
結合解離エネルギーとは、ホモリシスで特定の結合を分解するのに必要なエネルギー量である。
製品
結合エネルギー。
結合エネルギーは、結合形成の出発物質である原子を形成するのに必要なエネルギーを与える。
結合解離エネルギー。
結合解離エネルギーは、その特定の結合を形成した原子からフリーラジカルを形成するために必要なエネルギーを与える。
エネルギー価値
結合エネルギー。
結合エネルギー: 結合によって値が異なる。
結合解離エネルギー。
各結合で値は同じになる。
結論
結合エネルギーと結合解離エネルギーは、特定の化合物の生成や分解に必要なエネルギーを計算する上で重要である。
結合エネルギーと結合解離エネルギーは、一見同じように見えるが、2つの異なる形式です。
結合エネルギーと結合解離エネルギーの大きな違いは、結合エネルギーが化合物中の同じ2種類の原子間の結合をすべて分解するのに必要な平均的なエネルギー量であるのに対し、結合解離エネルギーはホモリシスで特定の結合を分解するのに必要なエネルギー量であることである。
つまり、結合エネルギーは、同じ種類の原子間に存在するすべての結合の結合解離エネルギーの平均値です。
