主な違い – 酢酸と氷酢酸の違い
酢酸は、エタン酸の通称です。
カルボン酸の一種で、カルボキシル基と-CH3基が結合したものです。
したがって、その化学式はC2H4O2です。
酢酸は、料理によく使われる家庭の必需品である酢によく含まれています。
氷酢酸は、酢酸を濃縮したものです。
酢酸と氷酢酸の大きな違いはその濃度にあり、酢酸溶液は水分を多く含むのに対し、氷酢酸は水分が1%以下です。
酢酸とは?
酢酸は無色透明で刺激臭のある溶液です。
酢の主成分です。
酢は約3~9%の酢酸を含んでいます。
酢酸は家庭や産業界で多くの用途があります。
料理、掃除、洗濯など、家庭で必要な多くの用途に使われます。
産業界では、酢酸は酢酸ビニル、無水酢酸、エステルなどの製造に使用されています。
酢酸の密度は1.04g/cm3です。
融点は約16.5度です。
以前は、酢酸はアセトアルデヒドの空気酸化、エタノールの酸化、ブタンの酸化によって工業的に作られていた。
しかし現在では、メタノールのロジウム-ヨウ素触媒によるカルボニル化反応によって、酢酸が工業的につくられている。
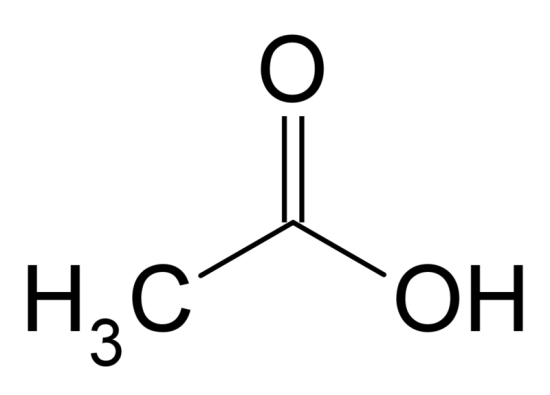 :図1 酢酸の化学構造
:図1 酢酸の化学構造
氷酢酸とは?
氷酢酸は、酢酸の純粋な形態です。
1%以下の水分で構成されています。
氷酢酸溶液中に存在する酢酸の量は約99.5%です。
氷酢酸は無色の液体で、非常に腐食性があります。
水と完全に混ざります。
氷酢酸は、そこに存在する水の量が非常に少ないため、無水(水を含まない)酢酸とも呼ばれています。
この酸は16.7℃付近で酢酸結晶に固化することができるので氷酢酸と呼ばれます。
この結晶は水より密度が高いので、容器の底に沈んでしまいます。
酢酸は食酢として食品に添加しても安全ですが、氷酢酸は腐食性があるため飲用には適しません。
氷酢酸の調製は、固形の氷酢酸の「鍾乳石」の上に酢酸溶液を浸すことで行うことができます。
すると、純粋な酢酸は氷酢酸に付着し、不純物は液体部分と一緒に流れ落ちます。
氷酢酸は、エステルの製造に非常に有効です。
エステルの製造には、氷酢酸とともに水を使用しますが、酢酸溶液中にすでに水があると、製造反応の平衡に影響を与え、最終的に得られるエステルの量が予想より少なくなってしまいます。
この場合、通常の酢酸水溶液よりも氷酢酸の方がはるかに優れています。
図2:16.5℃における氷酢酸の結晶生成の様子。
酢酸と氷酢酸の違い
定義
酢酸のこと。
酢酸は、酢酸と水を混ぜた溶液です。
氷酢酸。
氷酢酸は濃縮酢酸溶液です。
水分量
酢酸の場合 酢酸は水分を多く含み、希釈された状態です。
氷酢酸。
氷酢酸は水分が1%未満で、純酢酸を濃縮したものです。
使用方法
酢酸のことです。
酢酸は無害であり、食品添加物として使用される。
氷酢酸 腐食性が強く、触れると皮膚に傷をつけることがあります。
凍結
酢酸。
酢酸は凍結して結晶を作ることはない。
氷酢酸。
氷酢酸は16.5℃付近の低温で結晶を形成する。
生産
酢酸の製造 酢酸は、メタノールのロジウム-ヨウ素触媒によるカルボニル化反応により製造されます。
氷酢酸 氷酢酸は、固体氷酢酸の「鍾乳石」の上に酢酸溶液を浸漬することで製造することができます。
すると、純粋な酢酸は氷酢酸に付着し、不純物は液体部分と一緒に流れ落ちます。
結論
実験室内では、酸の種類に関わらず、取り扱いに注意が必要です。
酢酸は弱酸ですが、濃縮された状態では怪我をすることがあります。
この濃縮酢酸は、低温(16.5℃)で結晶を形成することから氷酢酸と呼ばれています。
酢酸と氷酢酸の大きな違いは、酢酸は酢酸溶液中に存在する水の量が多いのに対し、氷酢酸は水の量が1%以下であることです。
