酸性アミノ酸と塩基性アミノ酸の主な違いは、酸性アミノ酸は中性pHで酸性の側鎖を含むのに対し、塩基性アミノ酸は中性pHで塩基性の側鎖を含むことである。
さらに、酸性アミノ酸の側鎖はカルボン酸基を含み、塩基性アミノ酸の側鎖はアミノ基を含んでいる。
酸性アミノ酸、塩基性アミノ酸、中性アミノ酸は、側鎖または有機R基の極性に基づいて特徴づけられた3種類のアミノ酸です。
一般にアミノ酸は、中央の炭素原子にアミノ基(-NH2)、カルボキシル基(-COOH)、有機R基、水素原子が結合したものです。
主な対象分野
- 酸性アミノ酸とは?
– 定義、側鎖、重要性 - 塩基性アミノ酸とは
– 定義、側鎖、重要性 - 酸性アミノ酸と塩基性アミノ酸の類似点とは?
– 共通点の概要 - 酸性アミノ酸と塩基性アミノ酸の違いとは?
– 主な違いの比較
この記事の重要な単語
酸性アミノ酸、アミノ基、塩基性アミノ酸、カルボキシル酸基、極性
酸性アミノ酸とは?
酸性アミノ酸は、極性アミノ酸の一種で、側鎖にカルボキシル基(-COOH)を持つアミノ酸である。
つまり、アミノ酸の構造中にカルボキシル基が2つ含まれており、1つは側鎖に、もう1つは中心の炭素原子に結合している。
このため、溶液中のpKaが低下する。
したがって、酸性アミノ酸は側鎖のカルボキシル基からプロトンを失い、酸性の溶液を生成することができる。
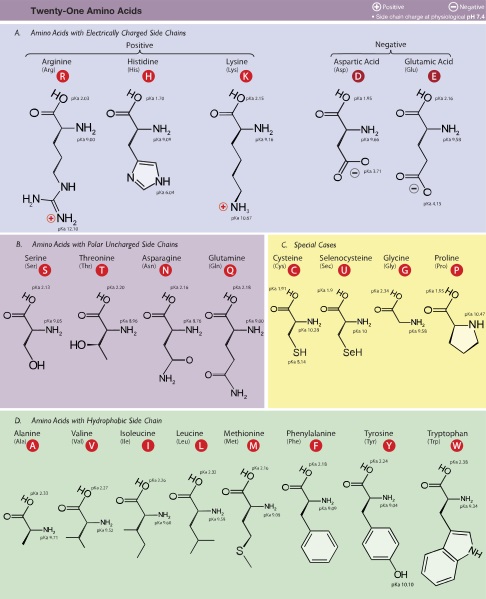 図1: アミノ酸の性質
図1: アミノ酸の性質
酸性アミノ酸は、主にグルタミン酸とアスパラギン酸の2種類があります。
基本アミノ酸とは何か
塩基性アミノ酸は、極性アミノ酸のもう一つのタイプです。
側鎖にアミノ基(-NH2)を持つ。
ここでも、塩基性アミノ酸は2つのアミノ基を持つ。
1つは側鎖に存在し、もう1つは中央の炭素原子に結合している。
したがって、酸性アミノ酸とは逆に、塩基性アミノ酸は高いpKaで構成されている。
このため、側鎖のアミノ基にプロトンを獲得することができ、塩基性溶液を生成することができる。
塩基性アミノ酸は、リジン、アルギニン、オルニチンの3種類であり、リジン、アルギニン、オルニチンは酸性アミノ酸です。
酸性アミノ酸と塩基性アミノ酸の類似性
- 酸性アミノ酸と塩基性アミノ酸は、有機R基の性質によって特徴づけられる2種類のアミノ酸です。
- 有機R基は、これらのアミノ酸で異なる極性で構成されている。
- 酸性アミノ酸と塩基性アミノ酸の間の水素結合は、βシートの形成に重要です。
- また、これらのアミノ酸は、タンパク質のサブユニット同士を結合し、タンパク質の三次構造を形成しています。
- さらに、両アミノ酸は、生体反応の酵素触媒反応において、様々な代謝物や酸性あるいは塩基性の中間体を安定化させる触媒部位としての役割を担っている。さらに、二次結合部位として、ATPの加水分解を安定化させる。
酸性アミノ酸と塩基性アミノ酸の違いについて
定義
酸性アミノ酸は、第二の酸部位を持つアミノ酸を指し、塩基性アミノ酸は、第二の塩基性基(通常はアミノ基)を持つアミノ酸を指します。
側鎖/有機R基
酸性アミノ酸と塩基性アミノ酸の大きな違いは、酸性アミノ酸は中性pHで酸性の側鎖を含み、塩基性アミノ酸は中性pHで塩基性の側鎖を含むことである。
サイドチェーンコンポーネント
酸性アミノ酸の側鎖にはカルボン酸基(-COOH)が含まれ、塩基性アミノ酸の側鎖にはアミノ基(-NH2)が含まれる。
したがって、この点も酸性アミノ酸と塩基性アミノ酸の違いです。
pKa
さらに、酸性アミノ酸はpKa値が低く、プロトンを失うことができ、塩基性アミノ酸はpKa値が高く、プロトンを結合させることができる。
チャージ
酸性アミノ酸と塩基性アミノ酸の違いとして、その電荷も挙げられる。
酸性アミノ酸は側鎖にマイナスの電荷を持ち、塩基性アミノ酸は側鎖にプラスの電荷を持っています。
例
酸性アミノ酸にはグルタミン酸やアスパラギン酸があり、塩基性アミノ酸にはリジン、アルギニン、オルニチンの3種類があります。
結論
酸性アミノ酸は、側鎖にカルボキシル基を持つため、マイナスの電荷を帯びることができる。
一方、塩基性アミノ酸は側鎖にアミノ基を持ち、正の電荷を帯びることができる。
この酸性アミノ酸と塩基性アミノ酸の電荷は、タンパク質の二次構造を形成する上で重要です。
また、酵素による生化学反応の触媒作用の際にも重要です。
したがって、酸性アミノ酸と塩基性アミノ酸の主な違いは、その側鎖に存在する官能基の種類にある。
