モル質量は物質の重要な物理的特性です。
密度、融点、沸点、系内で他の物質と反応する物質の量など、他の物理的・化学的性質の分析、比較、予測に非常に有用です。
今回は、原子量、方程式、沸点上昇、凝固点降下、浸透圧を用いた5種類の方法で、モル質量を計算する方法を紹介します。
モル質量とは
モル質量とは、特定の物質の1モルの質量のことです。
物質のモル質量の単位としては、gmol-1が最も一般的に使われています。
しかし、モル質量のSI単位はkgmol-1(またはkg/mol)です。
モル質量は次の式で計算できる。
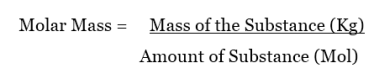
モルまたはモルは、物質の量を測定するために使用される単位です。
ある物質の1モルは、その物質が構成する原子(または分子)の6.023×1023個という非常に大きな数に相当する。
この数はアボガドロ数と呼ばれる。
原子の種類が何であれ、1モルはその量の原子(または分子)に等しいので、定数となります。
したがって、モル質量は新しい定義を与えることができます。
つまり、モル質量とは、ある特定の物質の6.023×1023個の原子(または分子)の総質量のことなのです。
混乱を避けるために、次の例を見てみましょう。
- 化合物AはAの分子で構成されている。
- 化合物BはBの分子で構成されている。
- 化合物Aの1モルは、Aの分子6.023×1023個で構成されている。
- 化合物Bの1モルは、B分子の6.023×1023で構成されています。
- 化合物Aのモル質量は、6.023×1023個のA分子の質量の合計です。
- 化合物Bのモル質量は、6.023×1023個のB分子の質量の総和です。
さて、これを実際の物質に当てはめてみましょう。
1モルのH2Oは6.023×1023個のH2O分子で構成されています。
6.023 x 1023個のH2O分子の質量の合計は約18gであるから、H2Oのモル質量は18g/molです。
モル質量の求め方
物質のモル質量は、いくつかの方法を用いて計算することができます。
- 方法1:原子量からモル質量を求める方法
- 方法2:方程式を使ってモル質量を計算する
- 方法3:沸点の上昇値からモル質量を算出する方法
- 方法4:凝固点降下量からモル質量を算出する方法
- 方法5:浸透圧からモル質量を算出する方法
これらの方法について、以下に詳しく説明します。
1. 原子量を用いたモル質量の求め方
分子のモル質量は、原子量を用いて求めることができる。
これは、存在する各原子のモル質量を足し合わせるだけでよい。
元素のモル質量は次のように表される。
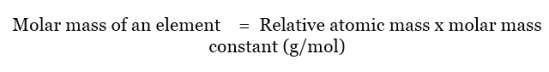
相対原子質量は炭素12原子の質量に対する原子の質量であり、単位はない。
この関係は次のように表されます。
モル質量の求め方 – 3
この手法を理解するために、次のような例を考えてみよう。
以下は、同じ原子の化合物、異なる原子の組み合わせ、多数の原子の組み合わせについて計算したものです。
計算例
1. H2 と HCl のモル質量の計算
モル質量の求め方 – 例題1
3. C6H12O6 のモル質量
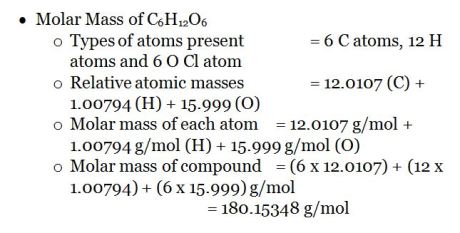
2. 式によるモル質量の求め方
モル質量は、以下の式で求めることができます。
この式は、未知の化合物を求めるときに使用する。
モル質量の求め方 – 4
計算例
次のような例を考えてみよう。
化合物Dは溶液の中にある。
その詳細は次のように示される。
- 化合物Dは強塩基です。
- 1分子につき1個のH+イオンを放出することができる。
- 化合物Dの溶液は、0.599gの化合物Dを用いて作られた。
- HClと1:1の割合で反応する。
そうすると、酸塩基滴定で定量できる。
強塩基なので、フェノールフタレイン指示薬の存在下、強酸(例:HCl、1.0 mol/L)で滴定する。
色の変化は滴定の終点(例:HCl 15.00mLを加えたとき)を示し、これで未知塩基の全分子が加えた酸で滴定されたことになる。
このとき、未知化合物のモル質量は、次のようにして求めることができます。
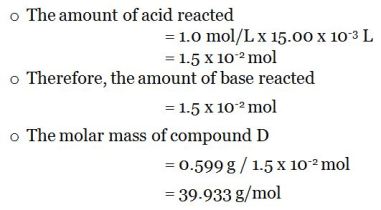
3. 沸点上昇からモル質量を求める方法
沸点上昇とは、純溶媒にある化合物を添加すると、その混合物の沸点が純溶媒の沸点よりも高くなることを示す現象です。
したがって、2つの沸点の温度差から、その添加化合物のモル質量を求めることができる。
純溶媒の沸点をTsolvent、溶液(化合物を加えたもの)の沸点をTsolutionとすると、2つの沸点の差は次のように与えることができる。
モル質量の求め方 – 01
クラウジウス・クラペイロンの関係やラウールの法則を用いると、ΔTと溶液のモル比の関係は次のようになります。
モル質量の求め方 – 02
ここで、Kbは溶媒の性質にのみ依存するエブリスコピック定数、Mはモル比を表します。
上の式から、溶液のモル比の値を求めることができます。
この溶液の調製に使用した溶媒の量がわかっているので、添加した化合物のモル数の値を求めることができる。
モル質量の求め方 – 5
溶液中の化合物のモル数と加えた化合物の質量がわかったので、式を使って化合物のモル質量を求めることができます。
モル質量の求め方 – 6
4.凝固点降下からモル質量を求める方法
凝固点降下は沸点上昇の逆です。
ある化合物を溶媒に加えたとき、その溶液の凝固点が純溶媒のそれよりも低くなることがあります。
その時は、上の式を少し修正する。
モル質量の求め方 – 03
沸点が初期値より低くなったので、ΔTの値はマイナスとなる。
沸点上昇法と同じ方法で溶液のモル%を求めることができる。
モル質量の求め方 – 04
ここで、Kfはクライオスコピック定数と呼ばれるものです。
これは溶媒の性質にのみ依存する。
その他の計算は沸点上昇法と同じです。
ここで、加えた化合物のモル数も下の式で計算できる。
モル質量の求め方 – 7
次に、加えた化合物のモル数と加えた化合物の質量の値からモル質量を計算することができます。
モル質量の求め方 – 8
5. 浸透圧からモル質量を求める方法
浸透圧とは、ある溶液に純溶媒が浸透して通過しないようにするために必要な圧力のことです。
浸透圧は次の式で与えることができる。
Π = MRT
Πを浸透圧としたとき。
Mは溶液のモル数
Rは普遍気体定数
Tは温度
溶液のモル比は次の式で与えられる。
モル質量の求め方 – 9
上記のように、溶液の体積を測定してモル量を計算することができます。
したがって、溶液中の化合物のモル数を測定することができる。
モル質量は式で求めることができる。
モル質量の求め方 – 8
なぜ物質のモル質量を知ることが重要なのか
- 異なる化合物のモル質量は、それらの化合物の融点と沸点を比較するために使用することができます。
- モル質量は、化合物に存在する原子の質量パーセントを決定するために使用されます。
- モル質量は、化学反応において、反応した特定の反応物の量を知るため、または得られる生成物の量を知るために非常に重要です。
- モル質量を知っておくことは、実験装置を設計する前に非常に重要です。
概要
ある化合物のモル質量を計算する方法はいくつかある。
その中で最も簡単な方法は、その化合物に含まれる元素のモル質量を足すことである。
