主な相違点 – SブロックとPブロックの元素
元素周期表には、これまでに発見されたすべての元素が記載されています。
これらの元素は、Sブロック、Pブロック、Dブロック、Fブロックという4つのグループに大別されます。
これらは、価電子が存在する軌道によって分類される。
さらに、これらの元素は、その物性によって、金属、非金属、金属化合物に分類される。
sブロックの元素は、水素を除いてすべて金属です。
pブロックの元素はほとんどが非金属です。
pブロックの残りの元素はメタロイドです。
sブロック元素とpブロック元素の主な違いは、sブロック元素の価電子がs軌道にあるのに対して、pブロック元素の価電子はp軌道にあることです。
Sブロック要素とは
Sブロック元素とは、価電子を最外周のS軌道に持つ元素のことです。
S軌道は最大2個の電子しか保持できないため、すべてのSブロック元素は最外周のS軌道に1個または2個の電子を持つ構成となっている。
その電子配置は常にs軌道(ns)で終わります。
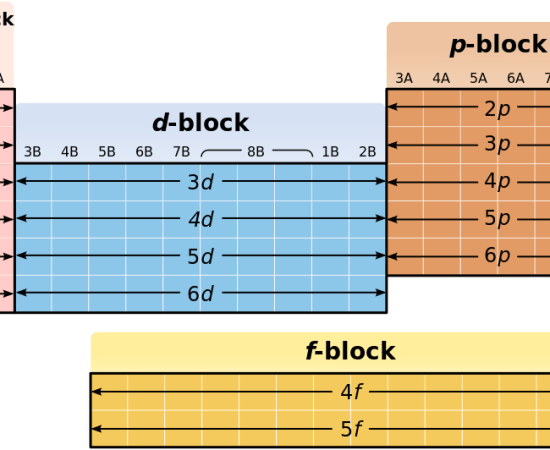 : 図1: 元素周期表のブロック (sブロックはピンク色)
: 図1: 元素周期表のブロック (sブロックはピンク色)
水素以外のsブロックはすべて金属です。
水素は非金属です。
水素は非金属ですが、s軌道しか持たないため、sブロックに分類されます。
1族と2族にはsブロックの元素が含まれます。
1A族の元素は一番外側のs軌道に1個の価電子を持つのに対し、2族の元素は2個の価電子から構成される。
1族元素はアルカリ金属、2族元素はアルカリ土類金属と命名されている。
ヘリウムも2個の電子で構成されるs軌道しか持たないので、sブロック元素と呼ばれる。
したがって、ヘリウムも価電子をs軌道に持ち、sブロック元素に分類されます。
また、ヘリウムは非金属です。
sブロック元素の酸化状態は、+1または+2です(水素は-1の場合もあります)。
これは、これらの元素は電子を1個(第1族元素)または2個(第2族元素)取り除くことで安定になるためです。
sブロック元素の原子半径は、各周期の後に新しい電子殻が追加されるため、グループ下で大きくなります。
原子半径が大きくなると、イオン化エネルギーは小さくなる。
これは、最外周の軌道にある電子が原子核に弱く引き寄せられるためです。
融点、沸点も同様に下降していく。
これは、原子半径が大きくなると、金属結合の強さが弱くなるためです。
したがって、金属原子は容易に分離することができる。
Pブロック要素とは
Pブロック元素とは、価電子を最外殻のP軌道に持つ元素のことです。
Pサブシェルは最大6個の電子を保持できる。
したがって、Pブロック元素の一番外側のp軌道にある電子の数は、1、2、3、4、5、6個のいずれかになります。
電子配置は常にp軌道(np)で終わっている。
pブロック元素の多くは非金属であるが、金属元素は少ない。
3族から8族までは、ヘリウムを除いてpブロック元素である(ヘリウムは前述のようにsブロックに属する)。
p ブロック元素の原子半径は、群から下に向かって大きくなり、周期に沿って小さくなります。
イオン化エネルギーは、群から下へ向かって減少し、周期に沿って増加する。
電気陰性度も周期に沿って増加する。
最も電気陰性度の高い元素はフッ素で、pブロックに属します。
pブロックの元素は、そのほとんどが同位体性を示します。
同位体性とは、同じ元素で分子構造の形が異なることを指す。
pブロック元素の酸化状態は、原子に存在する価電子の数によって変化することがあります。
酸化状態が1つしかない元素もあれば、複数の酸化状態を持つ元素もあります。
pブロックの第8族は希ガスで構成されています。
これらの元素は不活性ガスであり、極端な条件下でない限り化学反応を起こすことができない。
希ガスは最も安定な電子配置を持ち、p軌道は完全に電子で満たされています。
7族元素はハロゲンと呼ばれる。
pブロックのほぼすべての元素は共有結合を形成し、イオン結合にも関与することができる。
SブロックとPブロックの要素の違い
定義
Sブロック元素。
Sブロック元素とは、価電子が最外周のS軌道にある元素のこと。
Pブロック元素。
Pブロックとは、一番外側のP軌道に価電子を持つ元素のこと。
酸化状態
Sブロック元素。
Sブロック元素は0、+1、+2の酸化状態を持つ。
Pブロック元素。
Pブロック元素は-3、0から+5までの酸化状態(安定酸化状態)を示す。
化学結合
Sブロック元素。
Sブロック元素は金属結合とイオン結合を形成する。
Pブロック元素。
Pブロック:共有結合やイオン結合(金属との結合)を形成する。
金属特性
Sブロック元素。
Sブロックの元素はすべて金属です。
Pブロック元素。
Pブロック元素のほとんどは非金属で、その他は金属質です。
電気陰性度
Sブロック元素。
Sブロック元素の電気陰性度は比較的低い。
Pブロック元素。
Pブロックは比較的電気陰性度が高い。
結論
SブロックとPブロックは、元素の周期表で見られる化学元素です。
軌道上の価電子の位置によって、SブロックとPブロックに分類される。
sブロックとpブロックの主な違いは、sブロックの価電子がs軌道にあるのに対して、pブロックの価電子はp軌道にあることである。
