主な違い – ホウ砂対ホウ酸
ホウ砂とホウ酸は、他のいくつかの化学元素と一緒にホウ素原子で構成される2つの異なる化合物です。
ホウ砂は、ホウ酸ナトリウムに名前を付けるために使用される一般的な名前です。
これらは、その化学組成に応じて異なる化学的および物理的性質を有する。
ホウ砂は鉱物です。
それはホウ酸の塩です。
ホウ酸は、ホウ素の弱い一塩基性ルイス酸です。
殺虫剤、防腐剤、難燃剤など、さまざまな用途に使用されています。
ホウ砂とホウ酸の主な違いは、ホウ砂の化学式がNa2B4O7・10H2Oであるのに対し、ホウ酸の化学式はBH3O3であることです。
ホウ砂とは
ホウ砂は、化学式Na2B4O7・10H2Oで表される天然鉱物です。
ホウ酸ナトリウムとも呼ばれる。
しかし、この化合物のIUPAC名は四ホウ酸ナトリウム十水和物です。
ホウ素によって形成される非常に重要な化合物です。
ホウ砂のモル質量は、水和時381.38g/mol、脱水時201.22g/molです。
白色の固体として現れる。
無色透明の柔らかい結晶からなり、水に容易に溶ける。
結晶構造は単斜晶系プリズムです。
ホウ砂の融点は743℃、沸点は1,575℃です。
ホウ砂という用語は、ホウ酸ナトリウムのいくつかの密接に関連した化合物の名前に使用されます。
しかし、通常、ホウ酸ナトリウム単位あたり10個の水分子を持つ水和ホウ酸ナトリウム(四ホウ酸ナトリウム十水和物)に用いられることが多い。
この化合物の化学構造を考えると、4つのホウ素原子のうち2つが4つの座標結合を形成しているのに対し、他の2つのホウ素原子は3つの座標結合しか形成していない2種類のホウ素原子が存在することになる。
それぞれ四面体構造と三角形構造を持っています。
ホウ砂の利用法
ホウ砂は、次のように使用されます。
- 殺虫剤
- 殺真菌剤
- 除草剤
- 乾燥剤
- 家庭用洗剤
- 食品用防腐剤
ホウ酸とは
ホウ酸は化学式 BH3O3 で表されるホウ素のルイス酸です。
ホウ酸水素とも呼ばれる。
しかしホウ酸の IUPAC の名前は Trihydrooxidoboron です。
それは無色の水晶としてまたは白い粉としてあります。
ホウ酸のモル質量は61.83g/molです。
ホウ酸の融点は170.9℃であり、沸点は300℃です。
ホウ酸の化学構造は、三角形の平面構造をしている。
ホウ素に3個の不対電子しかないので、最大3個の共有結合を形成することができる。
ホウ酸では、ホウ素原子の周囲に3つの-OH基が存在する。
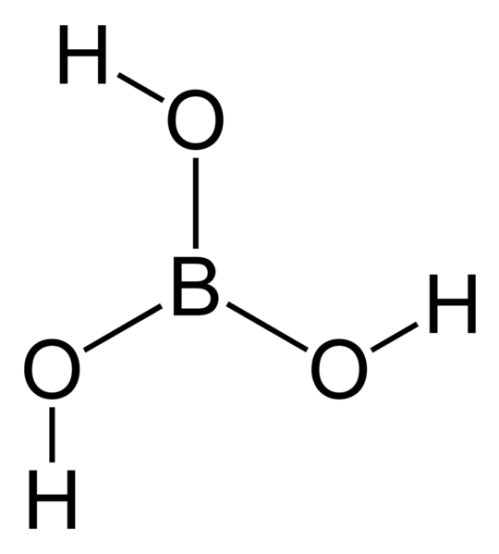
図2:ホウ酸の化学構造
ホウ酸は弱酸です。
ホウ素原子には電子が入ることのできる空の軌道があるため、ルイス酸と呼ばれる。
ルイス酸とは、ドナー化合物から電子対を受け取ることができる化合物またはイオン種のことである。
これは、水分子から-OH基が結合し、その電子対をホウ素の空の軌道に供与するためです。
ホウ酸は一塩基酸であり、交換可能な水素原子を1つだけ持っていることを意味します。
ホウ酸は、ホウ砂と塩酸などの鉱酸を反応させることで製造することができます。
その反応を以下に示します。
Na2B4O7-10H2O + 2HCl → 4B(OH)3 [またはH3BO3] + 2NaCl + 5H2O
ホウ酸の用途
- 防腐剤として
- 防カビ剤
- 難燃剤
- 中性子吸収剤
ホウ砂とホウ酸の違い
定義
ホウ砂:化学式Na2B4O7・10H2Oで表される天然鉱石。
ホウ酸。
ホウ酸は、化学式BH3O3で表されるホウ素のルイス酸です。
IUPAC名
ホウ砂:IUPAC名はSodium tetraborate decahydrate(四ホウ酸ナトリウム十水和物)です。
ホウ酸。
ホウ酸のIUPAC名は、トリヒドロキシドボロンです。
モル質量
ホウ砂:ホウ砂のモル質量は、水和物で381.38g/mol、脱水物で201.22g/molです。
ホウ酸。
ホウ酸のモル質量は61.83g/molです。
融点・沸点
ホウ砂:融点は743℃、沸点は1,575℃です。
ホウ酸。
ホウ酸の融点は170.9 ℃、沸点は300 ℃です。
自然
ホウ砂:ホウ砂は天然鉱石です。
ホウ酸。
ホウ酸は、弱い一塩基性ルイス酸です。
結論
ホウ砂とホウ酸はホウ素の化合物です。
ホウ砂は天然に存在する鉱物です。
ホウ砂は、塩酸などの鉱酸と反応させることでホウ酸を得ることができる。
ホウ酸は弱い一塩基性ルイス酸です。
ホウ砂とホウ酸の主な違いは、ホウ砂の化学式がNa2B4O7・10H2Oであるのに対し、ホウ酸の化学式はBH3O3であることです。
