主な違い – SN1 vs SN2 反応
有機化学における求核置換反応には、SN1とSN2という2つの種類があります。
しかし、SN1は単分子反応であり、反応速度はrate = K [R-LG]で表すことができます。
SN2はSN1と異なり、2分子反応を表し、反応速度は、rate = K’ [R-LG] [Nu-]で表すことができる。
また、SN1経路は多段階反応であり、SN2経路は単段階反応です。
これがSN1反応とSN2反応の大きな違いです。
SN1反応とは
有機化学における単分子求核置換反応を指す。
その反応機構の速度決定段階は、単一分子種の分解に依存する。
したがって、SN1反応の速度は rate = K [R-LG]で表すことができます。
さらに、SN1は多段階の反応であり、反応中に中間体やいくつかの遷移状態を形成する。
この中間体はより安定なカルボカチオンであり、分子の反応性はR-基に依存する。
下図にSN1反応の機構を示す。
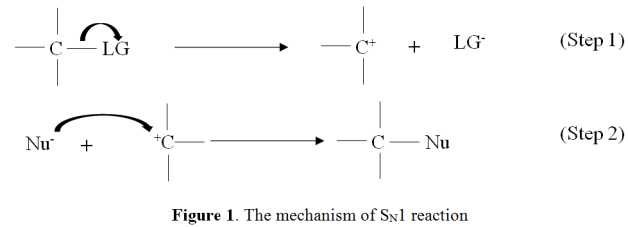
第一段階では、脱離基(LG)を失うことで、より安定なカルボカチオンが形成される。
これが最も遅いステップ、あるいは反応速度を決定するステップです。
その後、求核剤が親電子炭素を高速で攻撃し、新しい結合が形成される。
下図に示したSN1反応のエネルギープロファイルダイアグラムは、反応座標によるエネルギーの変化を表現している。
また、SN1反応の速度は、離脱基とアルキル側鎖の結合状態に依存する。
R-基の反応性を以下のように順序付けることができる。
反応性順序: (CH3)3C- > (CH3)2CH- > CH3CH2- > CH3-。
SN1反応では、脱離基が失われて中間体のカルボカチオンが形成されることが反応速度決定のステップとなる。
1級、2級、3級のうち、3級カルボカチオンは非常に安定であり、形成されやすい。
したがって、3級R基を持つ化合物はSN1反応の速度を向上させる。
同様に、脱離基の性質もSN1反応の速度に影響を与え、脱離基が良いほどSN1反応は速くなる。
しかし、求核剤は反応速度に関与しないので、求核剤の性質はSN1反応において重要ではない。
SN2反応とは
SN2 indicates the bimolecular nucleophilic substitution reactions in organic chemistry. In this mechanism, separation of leaving group and formation of new bond happen synchronously. Therefore, two molecular species involve with the rate determining step, and this leads to the term bimolecular nucleophilic substitution reaction or SN2. The rate of the SN2 reaction can be expressed by rate = K [R-LG] [Nu–]. In inorganic chemistry, this reaction also called “associative substitution” or “interchange mechanism.” The following figure illustrates the mechanism of SN2 reaction.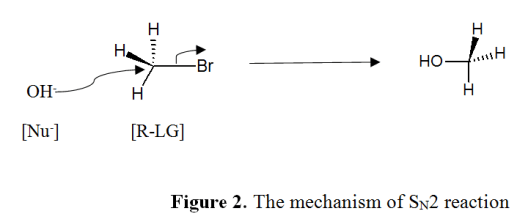
求核剤が脱離基の反対側を攻撃する反応です。
従って、SN2反応は常に立体化学の反転をもたらす。
この反応は、かさ高いアルキル基が求核剤の裏面攻撃を阻止するため、メチルやハロゲン化第1級化合物で最もよく機能する。
また、脱離基のアニオンとしての安定性と炭素原子との結合の強さは、いずれも反応速度に影響を与える。
下図にSN1反応とSN2反応のエネルギープロファイルダイアグラムを示します。
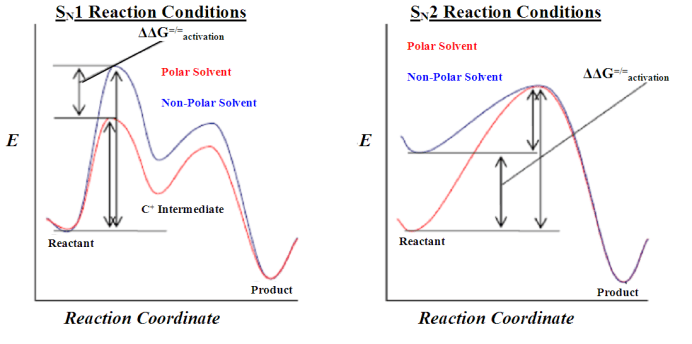
SN1反応とSN2反応の違い
レート法
SN1 反応。
SN1反応は単分子で一次反応です。
従って基質が反応速度に影響する。
SN2反応。
SN2 反応は二分子反応であり、二次反応です。
従って、基質と求核剤の両方が反応速度に影響を与える。
レート表現
SN1 反応。
rate = K [R-LG]で表される。
SN2反応。
反応速度=K’ [R-LG] [Nu-]で表される。
反応のステップ数
SN1 Reaction。
SN1 Reactionは1ステップのみです。
SN2 反応。
SN2 Reactionは2段階です。
カルボケーションの形成
SN1反応。
反応中に安定なカルボカチオンが生成する。
SN2反応。
離脱基の分離と新しい結合の形成が同時に起こるので、反応中にカルボカチオンは形成されない。
中間国
SN1反応。
一般に2つの中間状態を持つ。
SN2反応。
一般に中間状態が1つある。
反応のキーファクター/大きなバリア
SN1反応。
カルボカチオンの安定性が反応のキーファクターとなる。
SN2反応。
立体障害がキーファクター。
R基による反応性の順序
SN1反応。
SN2反応。
反応を進行させるための求核剤の必要量
SN1反応。
弱い求核剤または中性の求核剤が必要。
SN2反応。
強い求核剤が必要。
反応性の良い溶媒
SN1反応。
アルコールなどの極性プロトン性溶媒が好適。
SN2反応。
DMSO、アセトンなどの極性非プロトン性溶媒が好適。
立体化学
SN1反応。
立体化学的な保持や反転が起こりうるため、生成物はラセミ混合物となることがあります。
SN2 Reaction: Inversion of stereochemistry happens all the time.
「SN1反応とSN2反応における溶媒の効果” by Chem540f09grp12 – 自作 (Public Domain) via Commons Wikimedia
