主な違い – 共役と超共役
共役と超共役という用語は、不飽和有機化合物に関連している。
共役という言葉は化学的には異なる意味を持ち、2つの化合物が結合して1つの化合物を形成することを指す場合と、σ結合を挟んでp軌道が重なり合うことを指す場合があります。
今回は、共役とハイパーコンジュゲーション、すなわちσ結合とπネットワークの相互作用を比較しているので、共役の2番目の定義について考えてみることにする。
このように、コンジュゲーションとハイパーコンジュゲーションの大きな違いは、コンジュゲーションがσ結合を挟んだp軌道の重なりであるのに対して、ハイパーコンジュゲーションはσ結合とπネットワークの相互作用であることである。
コンジュゲーションとは
共役とは、σ結合(シグマ結合)を挟んでp軌道が重なり合うことです。
シグマ結合は共有結合の一種である。
二重結合を持つ不飽和化合物は、1つのシグマ結合と1つのπ結合で構成されている。
これらの化合物の炭素原子はsp2混成です。
sp2混成であるため、各炭素原子につき、未混成のp軌道が存在する。
単結合(シグマ結合)と二重結合(シグマ結合とπ結合)を交互に持つ化合物では、ハイブリッド化されていないp軌道同士が重なって、電子雲が形成されることがあります。
そして、そのp軌道上の電子は、この電子雲の内部で非局在化する。
このような非局在化した系を共役系と呼ぶ。
したがって、このようにp軌道が重なり合うことを共役系と呼ぶ。
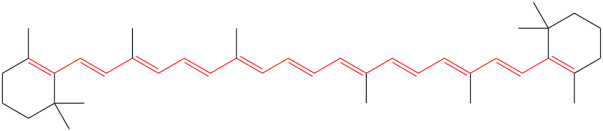 :図1 β-カロテン共役系
:図1 β-カロテン共役系
シグマ結合は、2つの原子軌道が正面からぶつかり合うことで形成される強い共有結合です。
最も単純な共有結合は、2つの原子のs軌道の間に形成される。
しかし、複雑な原子構造を持つ原子では、原子軌道が混成(原子軌道同士が混ざり合い、新しい形を持つ混成軌道を形成すること)している。
Sp2混成は、1つのs軌道と2つのp軌道が混成することである。
原子は3つのp軌道を持つので、sp2混成の後、混成されていないp軌道が残ります。
化合物の隣接するすべての炭素原子が未ハイブリッドのp軌道を持つ場合、これらの軌道は互いに重なり合うことができる。
これにより、共役系が形成される。
共役系は、環状化合物である芳香族化合物でも観察される。
ベンゼンは、共役π電子系を持つ芳香族化合物です。
ベンゼン環は6個の炭素原子がsp2混成してできている。
そのため、6個の炭素原子はすべて非ハイブリッドなp軌道を持つ。
これらの軌道は互いに重なり合い、共役系を形成している。
ハイパーコンジュゲーションとは?
ハイパーコンジュゲーションとは、πネットワークとσ結合の相互作用のことである。
シグマ結合の電子は、隣接する部分的に(あるいは完全に)満たされたp軌道、あるいはπ軌道と相互作用する。
ハイパーコンジュゲーションは、分子の安定性を高めるために起こる。
C-Hシグマ結合の結合電子が、隣接する炭素原子のp軌道やπ軌道と重なることによって、ハイパーコンジュゲーションが起こる。
水素原子はプロトンとして近傍に存在する。
炭素原子に発生した負電荷は、p軌道またはπ軌道の重なりにより非局在化する。
超共役は、化合物の化学的性質にいくつかの影響を与える。
例えば、カルボカチオンでは、超共役により炭素原子に正の電荷が発生する。
Conjugation と Hyperconjugation の違い
定義
共役。
共役とは、σ結合を挟んでp軌道が重なり合うこと。
ハイパーコンジュゲーション(Hyperconjugation) ハイパーコンジュゲーションとは、πネットワークとσ結合の相互作用のことである。
関与したコンポーネント
共役。
p軌道の間で共役を起こす。
ハイパーコンジュゲーション。
シグマ結合とp軌道またはπ軌道の間で超共役を起こす。
発生状況
Conjugation(共役)。
単結合と二重結合を交互に持つ化合物で起こる。
ハイパーコンジュゲーション。
カルボカチオンなど、C-H結合に隣接してp軌道やπ軌道を持つ化合物では、超共役を起こす。
成果
共役。
共役により、非局在化したπ電子雲が発生する。
ハイパーコンジュゲーション。
ハイパーコンジュゲーションにより、プロトンと安定化した分子が得られる。
結論
共役と超共役の2つの用語は、不飽和有機化合物を表す。
共役と超共役の主な違いは、共役はσ結合を挟んでp軌道が重なることであり、超共役はσ結合とπネットワークの相互作用であることである。
