主な違い – ヘリウム vs 水素
水素とヘリウムは、元素の周期表で最初に見つかる2つの元素です。
したがって、地球上で最も小さく、最も軽い原子です。
どちらも気体です。
水素とヘリウムの特徴から、これらの気体は産業界で多くの用途があります。
水素とヘリウムは非常に軽いため、気球の充填に利用されています。
ヘリウムと水素の主な違いは、ヘリウム原子が大気中で単原子ガスとして存在するのに対し、水素は大気中で2原子ガスとして存在することです。
ヘリウムとは
ヘリウムは原子番号2の元素で、気体の物質です。
ヘリウムの化学記号は He です。
ヘリウムの電子配置は 1s2 です。
ヘリウムの原子記号は42Heです。
ヘリウムの原子は、原子核の陽子2個と中性子2個、および1s軌道の電子2個で構成されています。
したがって、ヘリウムの原子質量は4.002602amuです。
常温常圧では、ヘリウムは無色無臭の気体です。
ヘリウムは宇宙で2番目に多く存在する元素と考えられている。
単原子ガスとして存在する。
ヘリウムの融点は約-272.2℃であり、非常に低い値です。
ヘリウムの沸点は-268oCとされている。
このため、より広い温度範囲に対応する気体です。
元素周期表では、ヘリウムはsブロック元素に分類されているが、表の右端に配置されている。
これは、ヘリウムが化学反応を起こさない不活性ガスであるためです。
また、非金属でもあります。
ヘリウムは希ガスなので、酸化状態はゼロしか示さない。
ヘリウムの同位体は2種類知られています。
3He同位体と4He同位体です。
4Heはその中で最も存在量が多く、その存在量は99%とされています。
この2つの同位体はともに安定で、放射性崩壊は観察されません。
しかし、他の同位体も存在します。
これらは不安定で放射性物質です。
ヘリウムは風船に広く使われています。
また、ヘリウムはその高い不活性度から、多くの合成反応(シリコン結晶の合成など)に制御された雰囲気を提供するために使用されています。
また、アーク溶接の不活性シールドとしても使用されている。
ヘリウムは液体にすることができ、これは液体ヘリウムと呼ばれ、重要な極低温材料として使用されている。
水素とは?
水素は原子番号1の化学元素で、Hという記号で表されます。
水素原子は原子核に陽子1個と中性子1個からなり、1s軌道に電子を1個持っています。
水素の電子配置は 1s1 となります。
水素は周期表ではsブロックの元素です。
水素の原子量は1.00794amuです。
常温常圧では、水素は2原子の気体分子として存在します。
無色・無臭の気体です。
水素の融点は約-259oCです。
沸点は約-252oCです。
水素には3つの酸化状態があります。
それらは-1、0、+1です。
水素が金属原子に結合している場合は、酸化状態が-1です。
水素には3つの主要な同位体があります。
プロチウム、重水素、三重水素です。
プロチウムは最も多い同位体で、その存在量は99%です。
したがって、一般に水素といえば、プロチウムのことを指します。
重水素も安定した同位体ですが、存在量は少なくなっています。
重水素は原子核に中性子を持ちますが、プロチウムにはありません。
トリチウムは放射性同位体です。
さらに、安定ではなく、放射性の高い同位体も多く存在します。
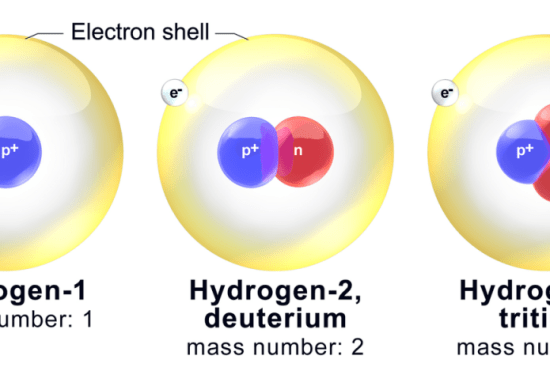 図2: 水素の主な同位体
図2: 水素の主な同位体
水素ガスにはさまざまな用途があります。
化石燃料の処理には大量の水素が使われる。
また、アンモニアの製造にも水素ガスが使われる。
さらに、発電所では冷却水としても利用されている。
ヘリウムと水素の共通点
- ヘリウムと水素は、標準的な温度と圧力の条件下では気体です。
- どちらも軌道が1sしかない。
- どちらも小さくて軽い物質です。
- どちらも周期律表のsブロックに属する元素です。
- どちらも非金属です。
ヘリウムと水素の違い
定義
ヘリウム ヘリウムは原子番号2の元素で、記号Heで表される。
水素:原子番号1の元素で、Hの記号で表される。
原子番号
ヘリウム ヘリウムの原子番号は2です。
水素 水素の原子番号は1です。
原子量
ヘリウム ヘリウムの原子量は、4.002602amuです。
水素。
水素の原子量は1.00794amuです。
化合物
ヘリウム ヘリウムは単原子の気体として存在する。
水素:水素は2原子の気体として存在する。
酸化状態
ヘリウム ヘリウムの酸化状態は0のみ。
水素:水素の酸化状態は、-1、0、+1 です。
同位体
ヘリウム ヘリウムには、3Heと4Heの2つの同位体があります。
水素:プロチウム、重水素、三重水素の3つの同位体があります。
融点
ヘリウム ヘリウムの融点は-272.2℃です。
水素 水素の融点は-259℃です。
結論
ヘリウムと水素は、融点や沸点が非常に低いため、大気中では主に気体として存在する化学元素です。
ヘリウムと水素の主な違いは、ヘリウム原子が大気中で単原子ガスとして存在するのに対し、水素は大気中で2原子ガスとして存在することである。
