遺伝地図と物理地図の主な違いは、遺伝地図の距離は遺伝的連鎖情報に依存するが、物理地図は塩基対の数で測定される実際の物理的距離に基づいていることである。
さらに、遺伝的地図では、遺伝マーカーと地図作成集団の大きさが重要な要素となる。
しかし、物理地図の場合、制限酵素による消化やゲノムの物理的な粉砕が必要である。
さらに、遺伝地図は染色体の様々な領域の性質についての洞察を与えることが多いが、物理地図はゲノムをより正確に表現している。
簡単に説明すると、遺伝地図と物理地図は、ゲノムマッピングに用いられる特徴的な2種類の地図です。
どちらも、ゲノム上のそれぞれの位置にある分子マーカーの集合を用いる。
主な対象分野
- 遺伝地図とは
– 定義、構造、重要性 - 物理地図とは
– 定義、構造、重要性 - 遺伝的マッピングと物理的マッピングの類似点とは?
– 共通点の概要 - 遺伝的マッピングと物理的マッピングの違いとは?
– 主な違いの比較
この記事の重要な単語
FISH、ジェネティックマッピング、ゲノムマッピング、マーカー、フィジカルマッピング、リストラクションマッピング、STSマッピング
ジェネティック・マッピングとは
遺伝子マッピングとは、染色体上の遺伝子の配置と相対的な距離を、組換え頻度を用いて明らかにする手法です。
このマッピングでは、遺伝子がマーカーとして機能するため、これらの地図は集団に特有です。
したがって、遺伝子地図の作成においては、作成母集団が重要な要素となる。
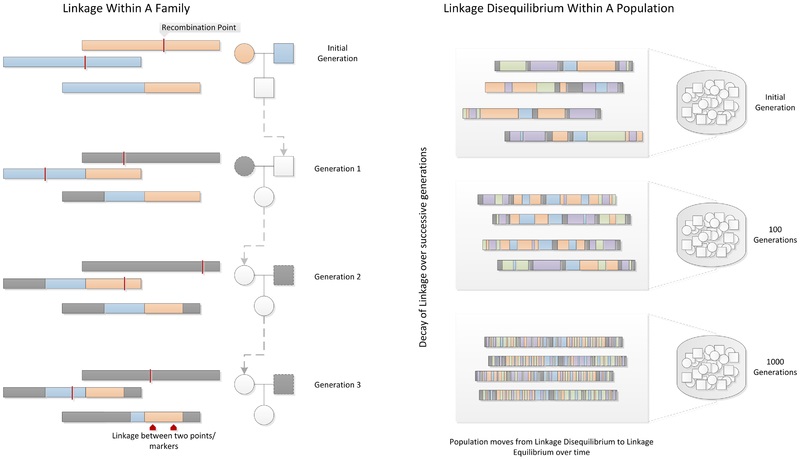
図1: 連鎖と連鎖不平衡
さらに、遺伝地図作成時には、遺伝子同士を比較することで、染色体上の遺伝子の順番を決定することができます。
また、遺伝子を解析することで、形質がどのように受け継がれるのか、どのように組み合わされるのかを調べることもできます。
マーカー
20世紀初頭、遺伝子はミバエのような生物の遺伝地図作成において、最初のマーカーとして機能した。
基本的に遺伝子はDNAの一部であり、親から子へ遺伝的特性を伝達する抽象的な存在です。
また、各遺伝子には少なくとも2つの対立遺伝子と呼ばれる代替形態があり、最終的に特定の表現型が生み出される。
そして、これらの表現型が視覚的な目印となり、体色、目の色、翅の形などの遺伝子の位置が示されたのが、最初のミバエの地図であった。
 :図2 トーマス・ハント・モーガンのキイロショウジョウバエ遺伝連鎖地図
:図2 トーマス・ハント・モーガンのキイロショウジョウバエ遺伝連鎖地図
しかし、その後、遺伝子地図は血液型診断のような生化学的な表現型に依存するようになった。
また、脊椎動物や顕花植物のゲノムのような大きなゲノムでは、他のDNA配列の特徴も有用です。
例えば、制限断片長多型(RFLP)、単純配列長多型(SSLP)、一塩基多型(SNP)です。
技術情報
遺伝地図作成の技術は、19世紀半ばにグレゴール・メンデルによって発見された遺伝学に由来する遺伝的連鎖に依存している。
メンデルの発見は、エンドウ豆を用いた育種実験の結果からなされた。
この実験では、ある遺伝子の2つの対立遺伝子が、ホモ接合体かヘテロ接合体のどちらかになることが示された。
さらに、この単純な優劣の法則の複雑な状況として、不完全優性、共優性などがあります。
さらに、第一法則では「対立遺伝子はランダムに分離する」、第二法則では「対立遺伝子の組は独立して分離する」とされているが、一般には染色体がそのまま遺伝の単位となり、その中の対立遺伝子の組が一緒に遺伝する、つまり部分連鎖があります。
この部分連結は、ハント・モーガンが述べた減数分裂における染色体の挙動を説明するものです。
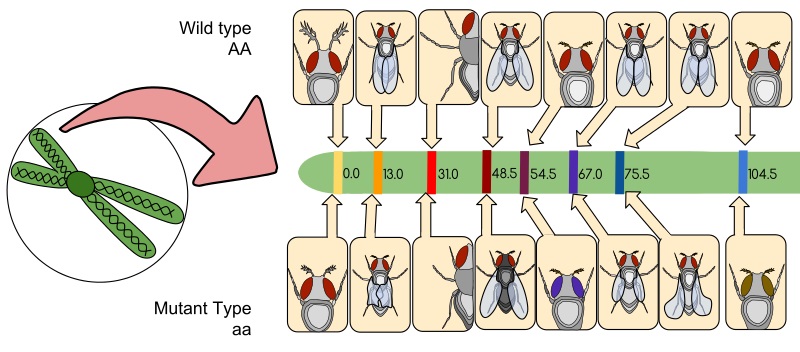 図3: クロスオーバー
図3: クロスオーバー
減数分裂の際に、染色体中のすべての対立遺伝子が一緒に受け継がれないことがあります。
実は、交叉はランダムな現象で、同じ染色体上の2つの遺伝子が相対的な距離によって分離することがあるのです。
そこで、組換え頻度を用いて、2つの遺伝子間の距離を決定することができる。
したがって、数対の遺伝子の組換え頻度を調べることで、遺伝地図を作成することができる。
また、植物では計画育種、ヒトでは血統解析が組換え頻度を求める方法です。
フィジカル・マッピングとは
一方、フィジカルマッピングは、2つの遺伝子の物理的な距離を示すために用いられる手法です。
一般に、遺伝子地図の解像度はクロスオーバーが少ないために低く、また精度にも限界があるため、物理マッピングが重要視されています。
また、マーカー間の実際の距離をヌクレオチドの数で示す。
基本的には、制限酵素マッピング、FISH (fluorescent in situ hybridization)、STS (sequence-tagged sites) マッピングなどが重要な手法です。
制限事項のマッピング
制限地図作成において、制限部位はDNAの目印となる。
このうち、多型制限部位は数少ないが、非多型制限部位は数多く用いられている。
一般に、制限地図を作成する最も簡単な方法は、DNA分子を異なる標的配列を持つ2種類の制限酵素で消化したときに生じる断片の大きさを比較することである。
しかし、制限地図の作成は、切断部位が比較的少ない短いDNA断片に適用される。
しかし、切断部位の少ないレアカッターを用いることで、50kb以上の大きなゲノム全体を解析できる可能性がある。
また、オプティカルマッピングは、染色した1分子のDNAから「オプティカルマップ」と呼ばれる秩序だったゲノム全体の高解像度制限地図を構築するもう一つの技術です。
図4: オプティカルマッピング
魚
蛍光in situハイブリダイゼーションは、染色体上のマーカーの位置を直接可視化することができる。
放射性プローブと蛍光プローブのハイブリダイゼーションを用いる。
また、染色体の凝縮度が高いメタフェースの染色体を使用する。
しかし、これは低解像度のマッピングにつながる。
そこで、機械的に伸長したメタフェース染色体や非メタフェース染色体を用いることで、分解能を向上させることができる。
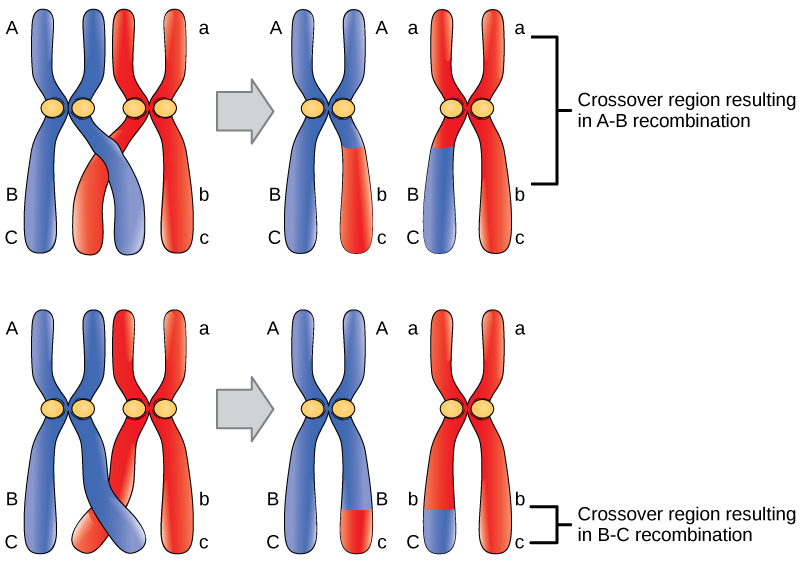 図5: FISH
図5: FISH
STSマッピング
Sequence Tagged mapping は、高解像度、高速、かつ技術的な負担が少ないマッピング手法です。
そのため、最も強力な物理的マッピング技術であり、大規模ゲノムの最も詳細な地図の作成を担ってきた技術です。
通常、STS(sequence-tagged site)は100~500bpの短いDNA配列で、特定の染色体やゲノムに一度だけ存在し、容易に認識することが可能である。
したがって、STSマップは、1つの染色体から採取した重複するDNA断片の集合体を用いて作成することができる。
遺伝的マッピングと物理的マッピングの類似性
- 遺伝的マッピングと物理的マッピングは、2種類のゲノムマッピング技術であり、それぞれ異なるタイプのゲノムマップを作成する。
- ゲノム上のそれぞれの位置にある分子マーカーのコレクションを使用する。
- どちらも、特定の表現型を生み出す遺伝子や、特定の変異を引き起こす変異を同定することができる。
- また、ゲノムマッピングは、多くの下流工程の初期過程です。
- 例えば、病気と関連する遺伝子の同定に役立ちます。
遺伝的マッピングと物理的マッピングの違い
定義
遺伝地図とは、染色体上の遺伝子マーカーの遺伝パターンから、その順序や相対的な距離を求めることを指す。
しかし、物理マッピングとは、DNAマーカーによるDNA塩基対の順序と物理的距離を求める手法のことである。
マーカの種類
遺伝子マッピングで用いるマーカーは遺伝子(遺伝マーカー)、物理マッピングで用いるマーカーは制限認識部位(DNAマーカー)です。
マーカーの意義
遺伝地図は遺伝的連鎖に依存するが、物理地図は短いDNA配列である視覚的マーカーを用いる。
頼りになる
遺伝地図は組換えと交叉に依存し、物理地図はゲノムのDNA配列に依存する。
技術情報
遺伝地図は組換え頻度に基づくが、物理地図は制限消化に基づく。
目的
遺伝地図は2点間の組換え事象の確率を決定し、物理地図は2点間の塩基数を決定する。
要因
遺伝的マッピングでは、遺伝マーカーとマッピング母集団の大きさが重要な要素です。
一方、物理的マッピングでは、制限消化または物理的にゲノムを断片化することが必要である。
精度
遺伝地図は、物理地図に比べ、比較的精度が低い。
重要性
遺伝地図は、1つの遺伝子(例:嚢胞性線維症、筋ジストロフィー)あるいは2つの遺伝子(例:糖尿病、癌、喘息)に関連する遺伝病について確固たる証拠を提供するものです。
一方、物理地図は、遺伝性疾患かランダムな突然変異による疾患かを問わず、疾患の起源を特定するのに重要です。
結論
遺伝地図は、遺伝子座の相対的な位置を、組換えの度合いに応じて表現する技術です。
したがって、遺伝子解析によって形質の遺伝や取り合わせを研究するものです。
従って、遺伝地図に使用されるマーカーの種類は遺伝子です。
これに対して、物理マッピングは、塩基の数で遺伝子座の実際の距離を求める手法です。
そのために、制限酵素消化やDNAシークエンスといった分子生物学の技術を用いる。
また、制限酵素の認識部位は、物理地図のDNAマーカーとして機能する。
そのため、遺伝的マッピングと物理的マッピングの主な違いは、マーカーの種類とマッピングに用いる技術です。
