主な相違点 – 付加反応と置換反応
付加反応、置換反応、脱離反応は、有機化学の基本的な反応です。
ほとんどの化学合成や同定は、これらの反応に基づいて行われます。
これらの反応は、1段階でも2段階でも起こります。
付加反応と置換反応の主な違いは、付加反応が2つ以上の原子または官能基の結合を伴うのに対し、置換反応は1つの原子または官能基が別の官能基によって置換されることである。
付加反応とは
付加反応とは、2つ以上の原子や分子が組み合わさって大きな分子を作ることです。
この大きな分子を付加体と呼びます。
付加反応の多くは、二重結合または三重結合を持つ不飽和の分子に限定される。
これらの付加反応は次のように分類される。
C
親電子性付加
求電子付加反応とは、親電子物質と分子が結合することである。
親電子性とは、電子を多く含む種から電子対を受け取り、共有結合を形成することができる原子または分子のことである。
親電子体は、より多くの電子を受け取るために、正電荷または中性電荷を持ち、電子を受け取るための自由な軌道を持つものです。
付加反応では副生成物は得られない。
上の例では、H+が求電子剤として作用します。
正電荷を帯びています。
二重結合のπ結合は電子が豊富です。
そこで、求電子剤(H+)は二重結合を攻撃し、その電荷を中和するための電子を獲得します。
上の例では、新しくできた分子は再び親電子派となる。
したがって、これも求電子的付加反応を起こすことができる。
求核付加反応
求核付加とは、求核剤と分子が結合することである。
求核剤とは、電子対を与えることができる原子または分子のことである。
求核剤は親電子剤に電子を供与することができる。
π結合を持つ分子、自由電子対を持つ原子や分子は求核剤として働く。
上の図では、「H2O」が求核剤であり、酸素原子に孤立電子対を持っています。
C原子は-C=O結合の極性により部分的に正電荷を帯びているため、中心の炭素原子にくっつくことができる。
フリーラジカル付加
フリーラジカル付加は、2つのラジカルの間、あるいはラジカルと非ラジカルの間に起こることがあります。
しかし、フリーラジカル付加は3つのステップを経て起こる。
- 開始 – ラジカルの形成
- 伝播 – ラジカルが非ラジカルと反応し、新たなラジカルを形成する。
- 終止 – 2つのラジカルが結合し、新しいラジカルの生成が終止する。
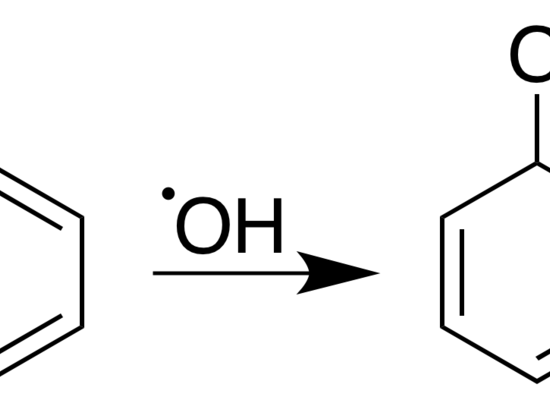 図03: “.OH “ラジカルとベンゼンの反応により、新しいラジカルが形成される。
図03: “.OH “ラジカルとベンゼンの反応により、新しいラジカルが形成される。
サイクロ加算
2つの環状または非環状分子の組み合わせから環状分子を生成することを環状付加反応という。
Diels-Alder反応は環状付加反応の好例です。
図4:シクロ付加の例
上の図は、カルボン酸化合物とアルケンの付加反応を示しています。
これらの付加により、環状化合物が生成している。
置換反応とは
置換反応とは、ある原子または原子団を別の原子または原子団で置き換える反応のことです。
その結果、脱離基と名付けられた副生成物が生じる。
置換反応の一般的な分類(置換基の種類による)を以下に示す。
- 求電子置換反応
- 求核置換反応
- ラジカル置換
親電子置換
求電子置換とは、原子または官能基を求電子剤で置き換えることである。
ここでいう求電子とは、電子を多く含む種から電子対を受け取ることができる原子または分子で、正電荷または中性電荷を帯びているものを指す。
上記の例では、ベンゼン環の水素原子1個がNO2+によって置換される。
ここで、NO2+基は正電荷を持つ求電子剤として作用する。
水素原子は脱離基となる。
求核置換
求核置換とは、原子または官能基を求核剤で置き換えることである。
ここでいう求核剤とは、電子対を与えることができ、負の電荷を持つ、または中性に帯電している原子または分子を指す。
上の図において、「Nu」は求核剤を示し、芳香族分子の「X」原子を置き換えます。
「X “原子は脱離基です。
ラジカル置換
ラジカル置換は、ラジカルと基質との反応を含む。
また、ラジカル置換では、反応の完結に少なくとも2段階(ラジカル付加反応と同じ)が必要である。
多くの場合、3つのステップが含まれる。
- 開始-ラジカルの生成
- 伝播-ラジカルが非ラジカルと反応し、新しいラジカルを形成する。
- 終結- 2つのラジカルが結合し、新たなラジカルの形成が終結する。
上の例では、メタンの水素原子が”.Cl “ラジカルに置換されている。
水素原子は脱離基です。
付加反応と置換反応の違い
定義
付加反応。
付加反応とは、2つ以上の原子や分子が組み合わさって大きな分子を形成すること。
置換反応。
置換反応とは、ある原子または原子団を別の原子または原子団で置き換える反応のことである。
最終分子
付加反応。
付加反応の後にできる大きな分子を付加体と呼ぶ。
置換反応。
求電子剤または脱離基を除いた分子部分を基質と呼ぶ。
副産物
付加反応。
付加反応では副生成物は生成しない。
置換反応。
置換反応では副生成物ができる。
副生成物は脱離基です。
基質または付加体のモル質量
付加反応。
付加反応の付加体のモル質量は、新しい原子や基が結合するため、常に最初の分子のモル質量より大きくなる。
置換反応。
置換反応では、置換基の種類によって、基質のモル質量は最初の分子より増加または減少することがあります。
結論
有機化学の反応機構を説明するために、付加反応と置換反応があります。
付加反応と置換反応の主な違いは、付加反応が2つ以上の原子または官能基の結合を伴うのに対し、置換反応は原子または官能基が他の官能基によって置換されることである。
